题目内容
2.(1)已知X、Y、Z为第三周期元素,其原子的第一至第四电离能如下:| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
(2)A、B、C、D是周期表中前10号元素,它们的原子半径依次减小.D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取SP3杂化.
①N是一种易液化的气体,请简述其易液化的原因氨分子间存在氢键,分子间作用力大因而易液化.
②W分子的VSEPR模型的空间构型为四面体型.
③写出AB-离子的电子式:[:C??N:]-.
(3))E、F、G三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4S1.
①E、F、G三元素的元素符号分别为K、、Cr、Cu.
②F元素在其化合物中最高化合价为+6.
③G2+离子的核外电子排布式为1s22s22p63s23p63d9或[Ar]3d9.G2+和N分子形成的配离子的结构式为
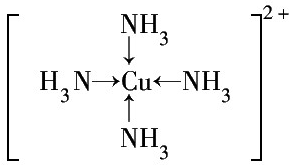 .
.
分析 (1)根据同周期元素的电离能判断元素的种类,X的I4电离能突然增大,说明最外层有3个电子,应为Al,Y的I3电离能突然增大,说明最外层有2个电子,应为Mg,Z的I2电离能突然增大,说明最外层有1个电子,应为Na;
(2)根据原子半径依次减小,D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取SP3杂化知,A、B、C、D分别为碳、氮、氧、氢.
①氨分子间存在氢键;
②根据价电子对互斥理论判断分子构型;
③含三键,满足8电子稳定结构;
(3)E、F、G分别为钾、铬、铜.
解答 解:(1)X的I4电离能突然增大,说明最外层有3个电子,应为Al,Y的I3电离能突然增大,说明最外层有2个电子,应为Mg,Z的I2电离能突然增大,说明最外层有1个电子,应为Na,由同周期从左向右原子半径减小可知,原子半径最小的为Al,三种元素中有两种元素的最高价氧化物对应的水化物能相互反应,离子反应为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al;Al(OH)3+OH-=AlO2-+2H2O;
(2)根据原子半径依次减小,D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取SP3杂化知,A、B、C、D分别为碳、氮、氧、氢.
①N为氨,是一种易液化的气体,是因为氨分子间存在氢键,分子间作用力大,因而易液化,故答案为:氨分子间存在氢键,分子间作用力大因而易液化;
②W为水,中心原子氧原子上有两对孤对电子,跟中心原子周围的σ键加起来是4,它们相互排斥,形成四面体,故水分子的VSEPR模型的空间构型为四面体,水分子的空间构型为V形,故答案为:四面体型;
③CN-离子的电子式为[:C??N:]-,故答案为:[:C??N:]-;
(3)E、F、G分别为钾、铬、铜.
①由上述分析可知,分别为K、Cr、Cu,故答案为:K、Cr、Cu;
②铬元素的价电子排布式为3d54s1,故其化合物中最高化合价为+6价,故答案为:+6;
③基态Cu的核外电子排布式为为[Ar]3d104s1,故Cu2+离子的核外电子排布式为[Ar]3d9,Cu2+和NH3分子形成的配离子为[Cu(NH3)4]2+,其结构式为 ,故答案为:1s22s22p63s23p63d9或[Ar]3d9;
,故答案为:1s22s22p63s23p63d9或[Ar]3d9; .
.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的性质、电子排布等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案| A. | 食盐 | B. | 火碱 | C. | 草木灰 | D. | 胆矾 |
| A. | 标准状况下,22.4L空气中O2、N2分子数为NA | |
| B. | 0.1mol羟基中所含电子数目为NA | |
| C. | 钠与氧气反应时,每消耗4.6g钠时生成的阴离子数目为0.1NA | |
| D. | 25℃时,1.0L pH=13的Ba(OH)2溶液中含有的OH-数为0.2NA |
| A. | 在常温常压下,2.24LSO2与O2混合气体中所含氧原子数为0.2NA | |
| B. | 50mL12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 标准状况下,20gD20分子中所含中子数为10NA |
| A. | NaHCO3溶液显弱酸性 | |
| B. | 该溶液中K+、Al3+、H+、SO${\;}_{4}^{2-}$可以大量共存 | |
| C. | 加水稀释该溶液,溶液中$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$增大 | |
| D. | 向该溶液中加入足量的氢氧化钙溶液的离子方程式为:2HCO${\;}_{3}^{-}$+Ca2++2OH-═CaCO3↓+CO${\;}_{3}^{2-}$+2H2O |
| A. | “山东疫苗案”涉疫苗未冷藏储运而失效,这与蛋白质变性有关 | |
| B. | 硫、氮、碳的氧化物是形成酸雨的主要物质 | |
| C. | 半导体行业中有一句“行话”:“从沙滩到用户”,说明计算机芯片的主要成分是二氧化硅 | |
| D. | 自来水厂常用明矾作消毒杀菌剂 |
| A. | 250mL | B. | 375mL | C. | 475mL | D. | 500mL |
 .固体甲溶于水后,溶液呈碱(酸、碱或中性),写出甲与水反应的化学方程式NH5+H2O=NH3•H2O+H2↑.
.固体甲溶于水后,溶液呈碱(酸、碱或中性),写出甲与水反应的化学方程式NH5+H2O=NH3•H2O+H2↑.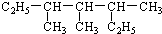 3,3,5-三甲基庚烷
3,3,5-三甲基庚烷