题目内容
如图是一个电化学过程的示意图,请回答下列问题: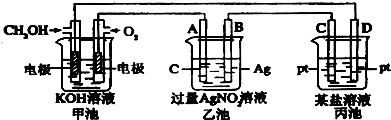
(1)图中甲池是 (填“原电池”“电解池”或“电镀池”).
(2)A(石墨)电极的名称是 (填“正极”“负极”“阴极”或“阳极”)
(3)写出通入CH3OH的电极的电极反应式
(4)乙池中反应的化学方程式为 当乙池中B(Ag)极质量增加54g,甲池中理论上消耗O2的体积为 L(标况).

(1)图中甲池是
(2)A(石墨)电极的名称是
(3)写出通入CH3OH的电极的电极反应式
(4)乙池中反应的化学方程式为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)图中甲池能自发进行氧化还原反应,属于原电池;
(2)通入甲醇的电极为负极、通入氧气的电极为正极,电解池中连接原电池负极的电极为阴极、连接原电池正极的电极为阳极;
(3)甲醇失电子和氢氧根离子反应生成碳酸根离子和水;
(4)乙池中A电极上氢氧根离子放电、阴极上银离子放电;根据转移电子相等计算消耗氧气体积.
(2)通入甲醇的电极为负极、通入氧气的电极为正极,电解池中连接原电池负极的电极为阴极、连接原电池正极的电极为阳极;
(3)甲醇失电子和氢氧根离子反应生成碳酸根离子和水;
(4)乙池中A电极上氢氧根离子放电、阴极上银离子放电;根据转移电子相等计算消耗氧气体积.
解答:
解:(1)图中甲池能自发进行氧化还原反应,将化学能转化为电能,所以属于原电池,故答案为:原电池;
(2)通入甲醇的电极为负极、通入氧气的电极为正极,A连接原电池正极,为电解池阳极,故答案为:阳极;
(3)甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3OH-6e-+8OH-═6H2O+CO32-,故答案为:CH3OH-6e-+8OH-═6H2O+CO32-;
(4)乙池中A电极上氢氧根离子放电、阴极上银离子放电,所以乙池电池反应式为4AgNO3+2H2O
4Ag+O2↑+4HNO3;B(Ag)极的质量增加54g时,n(Ag)=
=0.5mol,则转移电子为0.5mol,根据转移电子相等,则消耗氧气体积=
×22.4L/mol=2.8L,
故答案为:4AgNO3+2H2O
4Ag+O2↑+4HNO3;2.8.
(2)通入甲醇的电极为负极、通入氧气的电极为正极,A连接原电池正极,为电解池阳极,故答案为:阳极;
(3)甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3OH-6e-+8OH-═6H2O+CO32-,故答案为:CH3OH-6e-+8OH-═6H2O+CO32-;
(4)乙池中A电极上氢氧根离子放电、阴极上银离子放电,所以乙池电池反应式为4AgNO3+2H2O
| ||
| 54g |
| 108g/mol |
| 0.5mol |
| 4 |
故答案为:4AgNO3+2H2O
| ||
点评:本题考查了原电池和电解池原理,涉及电极反应式的书写及物质的量的金属,会结合电解质溶液酸碱性书写电极反应式,再结合转移电子相等进行计算,题目难度不大.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
若以R、M分别代表一种元素,结合元素周期表回答,下列说法正确的是( )
| A、若存在简单阴离子R-,则R一定属于ⅦA族 |
| B、若存在简单阴离子R2-,则R一定属于VIA族 |
| C、若存在简单阳离子M+,则M一定属于IA族 |
| D、若存在简单阳离子M2+,则M一定属于ⅡA族 |
下列各种方法中,能对金属起到防止或减缓腐蚀作用的是( )
①金属表面涂抹油漆 ②改变金属内部结构 ③保持金属表面清洁干燥 ④金属表面进行电镀 ⑤使金属表面形成致密的氧化物薄膜.
①金属表面涂抹油漆 ②改变金属内部结构 ③保持金属表面清洁干燥 ④金属表面进行电镀 ⑤使金属表面形成致密的氧化物薄膜.
| A、①②③④ | B、①③④⑤ |
| C、①②④⑤ | D、全部 |
 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.下列说法不正确的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.下列说法不正确的是( )| A、在正极发生的电极反应为:AgO+2e-+H2O=Ag+2OH- |
| B、在正极区H+浓度增大,在负极区H+浓度减少 |
| C、该电池总反应的化学方程式:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O |
| D、当电池负极的质量变化10.8g,则过程中电池流动的电子物质的量为1.2mol |
 硝酸是一种重要的化工原料,工业上生成硝酸的主要方法如下:
硝酸是一种重要的化工原料,工业上生成硝酸的主要方法如下:



 某课外活动小组用右图进行实验,试回答下列问题.
某课外活动小组用右图进行实验,试回答下列问题.