题目内容
20.元素A-D是元素周期表中短周期的四种元素,请根据表中信息回答下列问题.| 元素 | A | B | C | D |
| 性质 结构 信息 | 单质银白色,燃烧时火焰呈黄色. | 其单质是空气的主要成分,化学性质非常稳定. | 原子的3p亚层上有5个电子. | +2价阳离子的核外电子排布与氖原子相同. |
(2)A原子核外有4种能量不同的电子;写出D离子的核外电子排布式1s22s22p6.
(3)D和C形成的化合物R属于离子晶体;R的熔点高于四氯化碳,理由是R是离子晶体,固态四氟化碳是分子晶体
(4)A的金属性比D强,写出能证明该结论的一个事实金属钠能从熔融的氯化镁中置换出金属镁.
(5)设计一个简单实验,说明一水合氨是弱碱测定氯化铵溶液的pH值,测得其pH<7.
分析 A的单质银白色,燃烧时火焰呈黄色,则A为Na元素;B的单质是空气的主要成分,化学性质非常稳定,则B为N元素;C原子的3p亚层上有5个电子,则C原子含有3个电子层,最外层含有7个电子,为Cl元素;D的+2价阳离子的核外电子排布与氖原子相同,则D为Mg元素,据此结合元素周期律知识解答.
解答 解:(1)A的单质银白色,燃烧时火焰呈黄色,则A为Na元素;B的单质是空气的主要成分,化学性质非常稳定,则B为N元素;C原子的3p亚层上有5个电子,则C原子含有3个电子层,最外层含有7个电子,为Cl元素;D的+2价阳离子的核外电子排布与氖原子相同,则D为Mg元素,
根据分析可知,元素A、B、C、D分别为Na、N、Cl、Mg,
故答案为:Na;N;Cl;Mg;
(2)A原子为Na原子,钠原子核外电子有1s、2s、2p、3s,总共有4种;
D离子为镁离子,镁离子的核外电子总数为10,其核外电子排布式为:1s22s22p6,
故答案为:4;1s22s22p6;
(3)D、C形成的化合物为氯化镁,氯化镁为离子化合物,属于离子晶体;四氯化碳形成的晶体为分子晶体,氯化镁形成的晶体为离子晶体,所以氯化镁晶体的沸点大于四氯化碳晶体,
故答案为:离子;R是离子晶体,固态四氟化碳是分子晶体;
(4)由于金属钠能从熔融的氯化镁中置换出金属镁,说明Na的金属性大于Mg,
故答案为:金属钠能从熔融的氯化镁中置换出金属镁;
(5)测定氯化铵溶液的pH<7,说明氯化铵溶液中铵根离子部分水解,从而可证明一水合氨为弱碱,
故答案为:测定氯化铵溶液的pH值,测得其pH<7.
点评 本题考查了原子晶体与元素周期律的关系,题目难度中等,涉及电子排布式、金属性强弱判断、强弱电解质的判断、晶体类型及性质应用等知识,推断元素为解答关键,试题培养了学生的灵活应用能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案回答下列问题:
(1)SiH4的沸点比CH4高,原因是二者是结构相似的分子晶体,SiH4的分子量比CH4的分子量大,范德华力大,所以沸点比CH4高.
(2)硅与碳同主族,也有系列氢化物,但硅院在种类和数量上都远不如烷烃多.根据下表中所列键能数据,简要分析可能的原因Si-Si的键能比C-C小,Si-H的键能也比C-H小,更容易断裂,所以硅烷的种类和数量都比烷烃少.
| 化学键 | C-C | C-H | Si-Si | Si-H |
| 键能/(kJ•mol-1) | 356 | 413 | 226 | 318 |
3SiO2(s)+6C(s)+2N2(g) $\stackrel{高温}{?}$Si3N4(s)+6CO(g)
(3)标出上述反应中电子转移的数目和方向.
(4)该反应的平衡常数表达式K=$\frac{{C}^{6}(CO)}{C({N}_{2})}$.已知平衡常数:K(800℃)>K(850℃),则反 应是放热反应(填“放热”或“吸热”).
(5)任写两种能提高二氧化硅转化率的措施降温、减小压强.
(6)一定温度下,在2L密闭容器内,充入一定量的反应物,5分钟时达到平衡,测得容器内气体增加了0.4mol,用CO表示该反应时间内的反应速率为0.06mol/(L•min).
| A. | SO42- | B. | HCO3- | C. | SO32- | D. | Br- |
| A. | 质子数为8、中子数为10的氧原子:${\;}_{8}^{18}$O | |
| B. | 氧离子(O2-)的结构示意图: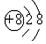 | |
| C. | 氧原子最外层p亚层电子排布式:2s22p4 | |
| D. | 某碳氧化合物电子式: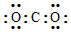 |
| A. | 正极 | B. | 负极 | C. | 阳极 | D. | 阴极 |
| A. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| B. | 中和滴定实验中,锥形瓶用蒸馏水洗净须经烤箱烘干后才可使用 | |
| C. | 配制0.5mol•L-1、480mL的NaOH溶液需称量9.6g的NaOH固体作溶质 | |
| D. | 某溶液中滴入2滴K3[Fe(CN)6]溶液生成具有特征蓝色的沉淀,说明原溶液中含有Fe2+ |
| A. | 0.01mol/L 标准盐酸溶液滴定未知浓度氨水,可以使用甲基橙作指示剂 | |
| B. | 向0.01mol/L酸性高锰酸钾溶液中滴加适量0.1mol/L草酸溶液,振荡,一段时间后溶液突然变为无色 | |
| C. | 向1mol/L KI溶液中逐滴滴加适量0.1mol/L稀硫酸和淀粉溶液,振荡,一段时间后无明显现象 | |
| D. | 向1mL 0.1mol/L MgCl2溶液的试管中滴加1~2滴2mol/L NaOH溶液,振荡后出现白色沉淀,再滴加2滴0.1mol/L FeCl3溶液,沉淀变为红褐色 |
| A. | Ne和Na+的结构示意图均为 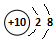 | B. | 聚氯乙烯的结构简式为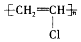 | ||
| C. | 二氧化碳分子的比例模型: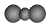 | D. | NH4Br的电子式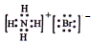 |
 NH4Al(SO4)2、NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下
NH4Al(SO4)2、NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下