题目内容
11.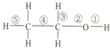 已知乙醇中不同的化学键如图,关于乙醇在各种不同反应中断裂的键的说明不正确的是( )
已知乙醇中不同的化学键如图,关于乙醇在各种不同反应中断裂的键的说明不正确的是( )| A. | 和浓H2SO4共热,140℃时键①②断裂 | B. | 在Ag催化下和O2反应键①③断裂 | ||
| C. | 和浓H2SO4共热,170℃时②⑤键断裂 | D. | 和氢溴反应键①断裂 |
分析 乙醇含有-OH,可发生取代、氧化和消去反应,可与钠反应,结合官能团的性质判断可能的共价键的断裂方式,以此解答.
解答 解:A.乙醇和浓H2SO4共热至140℃时,发生分子间脱水,生成乙醚,反应方程式为2CH3CH2OH $→_{140℃}^{浓硫酸}$CH3CH2O CH2CH3+H2O,故乙醇断键的位置为:①和②,故A正确;
B.在铜或银催化共热下与O2反应生成乙醛,则断裂①和③,故B正确;
C.乙醇和浓H2SO4共热至170℃时,发生消去反应,生成乙烯,反应方程式为CH3CH2OH $→_{170℃}^{浓硫酸}$CH2═CH2+H2O,故乙醇断键的位置为:②和⑤,故C正确;
D.和氢溴反应生成溴乙烷,键②断裂,故D错误.
故选D.
点评 本题考查有机物的结构和性质,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质和结构特点,学习中注意乙醇的性质,难度不大.

练习册系列答案
相关题目
19.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:1 下列说法正确的是( )
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 分子中一定含有氧原子 | D. | 此有机物的最简式为CH2 |
6.美国普度大学的研究人员开发出一种利用铝镓合金加水制造氢气的新工艺.这项技术具有广泛的能源潜在用途,包括为汽车提供原料、潜水艇提供燃料等.该技术通过向铝镓合金注水,铝生成氧化铝,同时生成氢气.合金中镓(Ga,ⅢA)是关键成分,可阻止铝形成致密的氧化膜.下列关于铝、镓的说法正确的是( )
| A. | 铝的金属性比镓强,铝的熔点比镓低 | |
| B. | 铝表面形成致密的氧化膜,所以可以用铝制容器来腌制咸菜 | |
| C. | Ga(OH)3与Al(OH)3性质相似,一定能与NaOH溶液反应 | |
| D. | 铝镓合金与水反应后的物质可以回收利用冶炼铝 |
3.五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构.A和B、D、E均能形成共价型化合物.A和B、C和E分别形成的化合物在水中均呈碱性.下列说法正确的是( )
| A. | 简单阳离子的氧化性:A>C | |
| B. | 可用单质的活泼性来比较B、D元素的非金属性 | |
| C. | 简单离子半径:C>D>E>B | |
| D. | E元素的某化合物A2E2O8中E的化合价为+7 |
20.NA为阿伏加德罗常数,下列物质的物质的量最小的是( )
| A. | 标准状况下2.24LO2 | B. | 含NA个氢原子的H2 | ||
| C. | 22gCO2 | D. | 含3.01×1023个分子的CH4 |
1.下列说法不正确的是( )
| A. | 常温下,在0.10mol•L-1CH3COOH溶液中加入少量CH3COONa晶体,能使CH3COOH的电离度降低,溶液的pH增大 | |
| B. | 常温下向氯化铵溶液中加入少量氨水使溶液中c(NH4+)=c(Cl-),则混合液的pH=7 | |
| C. | pH均为5 的盐酸和硫酸氢钠溶液中,水的电离程度后者大 | |
| D. | pH=3的0.1 mol•L-1HA溶液与0.05 mol•L-1NaOH溶液等体积混合后所得溶液中:2c(H+)+c(HA)=c(A-)+2c(OH-) |
 现用乙烯和其它无机物为原料合成环状有机物E(C6H8O4)的流程如下:
现用乙烯和其它无机物为原料合成环状有机物E(C6H8O4)的流程如下: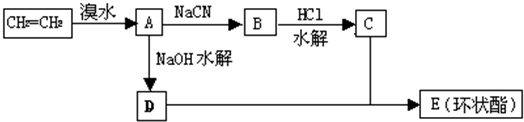
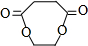 +2H2O.
+2H2O.