题目内容
1.硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸、硫代硫酸(H2S2O3) 等等,其中硫酸最为重要,在工业上有广泛的应用,在实验室,浓硫酸是常用的干燥剂.(1)焦硫酸(H2SO4•SO3)溶于水,其中的SO3都转化为硫酸,若将890g焦硫酸溶于水配成8.00L硫酸,该硫酸的物质的量浓度=1.25mol•L-1;
(2)若以浓硫酸吸水后生成H2SO4•H2O计算,500g质量分数为98%的硫酸能吸收水的质量=80g.
分析 (1)根据焦硫酸(H2SO4•SO3)溶于水,其中SO3都转化为硫酸,即n(H2SO4)=2n(H2SO4•SO3),结合公式c=$\frac{n}{V}$来求硫酸的物质的量浓度;
(2)根据浓硫酸吸水后生成H2SO4•H2O计算,硫酸与水的物质的是为1:1.
解答 解:(1)n(H2SO4)=2n(H2SO4•SO3)=$\frac{890g}{178g/mol}$×2=10mol,所以该硫酸的物质的量浓度为c(H2SO4)=$\frac{10mol}{8.00L}$=1.25mol/L,
故答案为:1.25;
(2)n(H2SO4•H2O)=n(H2SO4)=$\frac{500g×98%}{98}$=5mol,所以吸收水的质量为:5mol×116g/mol-500g=80g,
故答案为:80g.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确物质的量浓度的概念及表达式即可解答,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
12.某温度下,H2(g)+CO2(g)??H2O(g)+CO(g)的平衡常数K=$\frac{9}{4}$,该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示,下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol•L-1 | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol•L-1 | 0.010 | 0.010 | 0.020 |
| A. | 平衡时,乙中CO2的转化率大于60% | |
| B. | 平衡时,甲中和丙中H2的转化率均是60% | |
| C. | 平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol•L-1 | |
| D. | 反应开始时,丙中的反应速率最快,甲中的反应速率最慢 |
16.借助新的显微技术,能成功观察到小于200nm的粒子.下列分散系中,分散质粒子半径最大的是( )
| A. | 雾 | B. | 蛋白质溶液 | C. | 石灰乳 | D. | 硝酸钾溶液 |
13.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 18gH2O含有的氢原子数目为NA | |
| B. | 标准状况下,22.4LCO2含有的分子数目为NA | |
| C. | 1mol H2O在标准状况下的体积为22.4 L | |
| D. | 1L 1mol•L-1K2SO4溶液中含有的钾离子数目为NA |
10.下列各组溶液中,只用试管和胶头滴管,不用其他任何试剂就可以鉴别的是( )
| A. | KOH和AlCl3 | B. | 稀盐酸和NaOH | C. | CaCl2和Na2CO3 | D. | Ba(OH)2和NaHSO4 |
 、
、 、
、 .
.

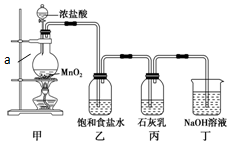 某兴趣小组设计了下列实验装置探究氯气与石灰乳反应的条件和产物.
某兴趣小组设计了下列实验装置探究氯气与石灰乳反应的条件和产物.