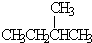题目内容
在密闭容器中将CO和水蒸气的混合物加热到800℃时,有下列平衡:CO+H2O?CO2+H2,且K=1.若用2molCO和10mol H2O相互混合并加热到800℃,则CO的转化率为( )
| A、16.7% | B、50% |
| C、66.7% | D、83.3% |
考点:化学平衡的计算
专题:化学平衡专题
分析:依据化学平衡的三段式列式计算,结合平衡常数表达式计算消耗的一氧化碳的物质的量,结合转化率概念计算得到,反应前后气体物质的量不变,可以利用气体物质的量代替平衡浓度计算平衡常数;
解答:
解:在密闭容器中将CO和水蒸气的混合物加热到800℃时,达到平衡状态,设消耗一氧化碳物质的量为x:
CO+H2O?CO2+H2,
起始量(mol) 2 10 0 0
变化量(mol) x x x x
平衡量(mol)2-x 10-x x x
反应前后气体物质的量不变,可以利用气体物质的量代替平衡浓度计算平衡常数
平衡常数K=
=1.
x=
mol
则CO的转化率=
×100%=83.3%;
故选D.
CO+H2O?CO2+H2,
起始量(mol) 2 10 0 0
变化量(mol) x x x x
平衡量(mol)2-x 10-x x x
反应前后气体物质的量不变,可以利用气体物质的量代替平衡浓度计算平衡常数
平衡常数K=
| x×x |
| (2-x)(10-x) |
x=
| 5 |
| 3 |
则CO的转化率=
| ||
| 2mol |
故选D.
点评:考查了化学平衡计算方法的分析应用,主要是平衡常数概念的计算,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列离子方程式中正确的是( )
| A、稀硫酸与氢氧化钡溶液反应 H++OH-=H2O |
| B、硫酸铝溶液中滴入氨水 Al3++OH-=Al(OH)3↓ |
| C、将足量CO2通入偏铝酸钠溶液中 Al3++CO2+H2O=Al(OH)3↓+CO32- |
| D、硝酸铝溶液中滴加少量氢氧化钠溶液 Al3++3OH-=Al(OH)3↓ |
Fe与稀H2SO4反应制取氢气,下列措施一定能使生成氢气的速率加快的是( )
| A、增加铁的量 | B、增大硫酸的浓度 |
| C、加热 | D、增大压强 |
某温度下,将等物质的量的P与Q投入体积固定2L密闭容器中,发生反应2P(g)+Qg)?xW(g)+U(g),经5min后到达平衡,这5min内W的平均反应速率是0.2mol/(L?min),平衡时U的浓度为0.5mol/L,[P]:[Q]=1:2,下列说法中不正确的是( )
| A、x值是2 |
| B、P平衡转化率为66.7% |
| C、平衡常数为1 |
| D、反应前,Q的物质的量为3 mol |
氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
| A、都不稳定 |
| B、能透过滤纸 |
| C、分散质粒子直径在1 nm~100 nm之间 |
| D、呈红褐色 |
如图,下列叙述正确的是( )
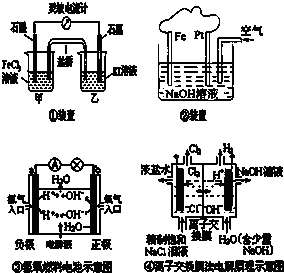

| A、①装置的总反应为2Fe3+2I-═2Fe2++I2 |
| B、②装置中Fe为阴极,电极反应为 Fe-2e-+2OH-═Fe(OH)2 |
| C、③装置中外电路电子由b极流向a极 |
| D、④装置的离子交换膜允许阳离子、阴离子、水分子自由通过 |
根据阿伏加德罗定律,下列叙述中正确的是( )
| A、同温同压下两种气体的体积之比等于摩尔质量之比 |
| B、同温同压下两种气体的质量之比等于物质的量之比 |
| C、同温同压下两种气体的物质的量之比等于密度之比 |
| D、同温同压下两种气体的摩尔质量之比等于密度之比 |
下列说法中正确的是( )
| A、用苯萃取碘水中的碘时,应先打开上端玻璃塞再将苯层从分液漏斗下口放出 |
| B、用湿润的红色石蕊试纸检验氨气 |
| C、稀释浓硫酸时,应将浓硫酸沿玻璃棒缓慢注入盛水的量筒中 |
| D、用广泛pH试纸测得0.1 mol?L-1NH4Cl溶液的pH=5.2 |
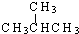 和
和 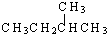 ②
② 和
和