题目内容
14.120℃时,氢气和氧气的混合气体共10L,充分反应后体积为7L(同温、同压),氢气和氧气的体积各为多少?分析 该温度下反应方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O(g),根据方程式知,反应前后气体体积减少参加反应的混合气体的$\frac{1}{3}$,据此分析解答.
解答 解:该温度下反应方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O(g),根据方程式知,反应前后气体体积减少参加反应的混合气体的$\frac{1}{3}$,反应后气体减少体积=(10-7)L=3L,
1.假设氢气过量,反应前后减少的体积为氧气体积,则氧气体积为3L、氢气体积为7L;
2.假设氧气过量,反应前后减少的体积为氢气的一半,反应前后气体减少体积为3L,则氢气体积为6L,氧气体积为4L,
答:氢气和氧气体积分别为7L、3L或6L、4L.
点评 本题考查方程式的有关计算,侧重考查学生分析计算能力,为高频考点,采用假设法分析解答,因为很多同学往往漏掉一种情况而导致错误,题目难度不大.

练习册系列答案
相关题目
4.下列关于糖类、油脂、蛋白质的说法正确的是( )
| A. | 蔗糖在人体内水解产物只有葡萄糖 | |
| B. | 油脂水解可得到氨基酸和甘油 | |
| C. | 淀粉和纤维素水解最终产物都是葡萄糖 | |
| D. | 鉴别部分蛋白质可利用浓硫酸与蛋白质的颜色反应 |
2.下列说法中正确的一组是( )
| A. | H2和D2互为同位素 | |
| B. | CH3-CH2-OH与CH3-O-CH3互为同分异构体 | |
| C. | 正丁烷和异丁烷是同系物 | |
| D. | ${\;}_{8}^{16}$O、${\;}_{8}^{17}$O、${\;}_{8}^{18}$O互为同素异形体 |
9.将0.01mol NaOH和0.01mol Na2CO3混合并配成溶液,滴加amL、0.1mol•L-1稀盐酸,下列说法不正确的是( )
| A. | 当a≤100时,发生的离子反应为:OH-+H+=H2O | |
| B. | 当a≥300时,发生的离子反应为:OH-+3H++CO32-=2H2O+CO2↑ | |
| C. | 当100<a<200时,反应后的溶液中CO32-与HCO3-的物质的量之比为(a×10-4-0.01):(0.02-a×10-4) | |
| D. | 当a=200时,发生的离子反应为:OH-+2H++CO32-=H2O+HCO3- |
7.如图表示一定条件下反应N2(g)+3H2(g)?2NH3(g)△H<0的反应速率与反应过程的曲线关系图.下列说法正确的是( )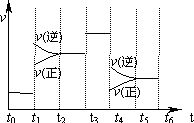

| A. | t2~t3和t3~t4时间段氨气的体积分数相等 | |
| B. | 氨气的体积分数最高的一段时间为t5~t6 | |
| C. | t4时刻改变的条件是降低温度 | |
| D. | t4~t5时间段平衡向正反应方向移动 |
4.表列出了A~R十种元素在周期表的位置:
(1)写出R单质分子的结构式N≡N
(2)A、C、D 三种元素的最高价氧化物对应的水化物中碱性最强的是NaOH(填化学式).
(3)A、B、C 三种元素的阳离子按离子半径由大到小的顺序排列为K+>Na+>Mg2+.(用元素的离子符号表示).
(4)X 元素是 A~R 十种元素中的一种,X 的氢氧化物既能与氢氧化钠溶液反应,又能与盐酸反应.则 X 的最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
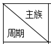 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
(2)A、C、D 三种元素的最高价氧化物对应的水化物中碱性最强的是NaOH(填化学式).
(3)A、B、C 三种元素的阳离子按离子半径由大到小的顺序排列为K+>Na+>Mg2+.(用元素的离子符号表示).
(4)X 元素是 A~R 十种元素中的一种,X 的氢氧化物既能与氢氧化钠溶液反应,又能与盐酸反应.则 X 的最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
5.由H2与CO组成的混合气体1.5g,在标准状况下其体积为2.24L,则混合气体中H2的物质的量为( )
| A. | 0.01mol | B. | 0.03mol | C. | 0.05mol | D. | 0.07mol |