题目内容
下列有关说法正确的是( )
| A、TATP(C8H18O6)受撞击分解爆炸,且无明显热效应,说明该分解反应熵显著增加 |
| B、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
| C、pH=3的盐酸与pH=11的LiOH溶液等体积混合溶液呈碱性,说明LiOH为强碱 |
| D、Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解程度减小,溶液的pH减小 |
考点:反应热和焓变,弱电解质在水溶液中的电离平衡,盐类水解的应用
专题:基本概念与基本理论
分析:A、该反应自发进行,说明△H-T△S<0;
B、CH3COONH4溶液中,醋酸根和铵根都会水解,溶液显中性说明水解程度相同;
C、盐类水解规律是“谁弱显谁性”;
D、因为生成NaOH,溶液pH增大.
B、CH3COONH4溶液中,醋酸根和铵根都会水解,溶液显中性说明水解程度相同;
C、盐类水解规律是“谁弱显谁性”;
D、因为生成NaOH,溶液pH增大.
解答:
解:A、该反应自发进行,说明△H-T△S<0,且无明显热效应,说明该分解反应熵显著增加,故A正确;
B、NaCl溶液中,无可以水解的离子,水正常电离;而CH3COONH4溶液中,醋酸根和铵根都会水解,溶液显中性说明水解程度相同,但水的电离程度增大,故B错误;
C、盐类水解规律是“谁弱显谁性”,LiCl溶液显碱性,说明,说明LiOH为弱碱,故C错误;
D、两溶液反应生成CaCO3沉淀和NaOH,所以,CO32-水解程度减小,溶液的pH增大,故D错误.
故选:A.
B、NaCl溶液中,无可以水解的离子,水正常电离;而CH3COONH4溶液中,醋酸根和铵根都会水解,溶液显中性说明水解程度相同,但水的电离程度增大,故B错误;
C、盐类水解规律是“谁弱显谁性”,LiCl溶液显碱性,说明,说明LiOH为弱碱,故C错误;
D、两溶液反应生成CaCO3沉淀和NaOH,所以,CO32-水解程度减小,溶液的pH增大,故D错误.
故选:A.
点评:本题考查反应自发进行的条件、影响盐类水解的因素、盐类水解对溶液酸碱性的影响等,题目难度不大.

练习册系列答案
相关题目
下列叙述中,正确的是( )
| A、乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |
| B、聚乙烯可发生加成反应 |
| C、所有的糖类、油脂和蛋白质都能发生水解反应 |
| D、符合分子式C4H10的物质有4种 |
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.下列叙述正确的是( )
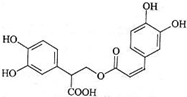

| A、迷迭香酸可以发生取代、水解、酯化和皂化反应 |
| B、1mol迷迭香酸最多能和9mol氢气发生加成反应 |
| C、1mol迷迭香酸最多能和含5mol NaOH水溶液完全反应 |
| D、1mol迷迭香酸最多能和含7mol Br2的溴水完全反应 |
区别SO2与CO2可用的方法是( )
| A、品红溶液 |
| B、澄清石灰水 |
| C、紫色石蕊试液 |
| D、BaCl2溶液 |
根据下表信息,判断以下叙述正确的是( )
表:部分短周期元素的原子半径及主要化合价
表:部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A、氢化物的沸点为H2T<H2R |
| B、M、Q元素的金属性 L<M |
| C、工业上通过电解L与T形成的化合物生产单质L |
| D、离子半径:R2->T2->L2+>M3+ |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、12g金刚石中所含共价键数目为2NA |
| B、含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA |
| C、标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA |
| D、46g NO2和N2O4的混合物含有的分子数为NA |
下列各组中的性质比较,正确的是( )
①酸性:HClO4>HBrO4>HIO4 ②碱性:KOH>Ca(OH)2>Mg(OH)2
③稳定性:HCl>H2S>PH3 ④还原性:F->Cl->Br-.
①酸性:HClO4>HBrO4>HIO4 ②碱性:KOH>Ca(OH)2>Mg(OH)2
③稳定性:HCl>H2S>PH3 ④还原性:F->Cl->Br-.
| A、①②④ | B、②③④ |
| C、①②③ | D、都正确 |
下列反应离子方程式正确的是( )
| A、溴化亚铁溶液中通入过量氯气:Fe2++2Br-+2Cl2=Fe3++Br2+4Cl- |
| B、氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O |
| C、向澄清石灰水中加入少量小苏打溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| D、氨水中通入过量二氧化硫:2NH3?H2O+SO2=2NH4++SO32-+2H2O |
圆底烧瓶中加入的反应物是溴化钠、乙醇和1:1的硫酸.配制体积比1:1的硫酸所用的定量仪器为 ( )(选填编号).
| A、天平 | B、量筒 |
| C、容量瓶 | D、滴定管. |