题目内容
16.写出明矾净水的原理,用离子方程式解释Al3++3H2O?Al(OH)3(胶体)+3H+.分析 明矾净水原理是电离出的铝离子水解生成氢氧化铝胶体具有吸附性,据此分析.
解答 解:明矾净水原理是硫酸铝钾溶液中含有铝离子,铝离子水解Al3++3H2O?Al(OH)3(胶体)+3H+,生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性净水,
故答案为:Al3++3H2O?Al(OH)3(胶体)+3H+.
点评 本题考查了盐类水解离子方程式的书写,把握明矾净水原理为解答的关键,注意根据反应原理找出反应物、生成物、反应条件,题目难度不大.

练习册系列答案
相关题目
6.氮分子中的化学键是( )
| A. | 3个σ键 | B. | 1个σ键,2个π键 | C. | 3个π键 | D. | 1个σ键,1个π键 |
7.下列分子中,核磁共振氢谱中有3个峰的是( )
| A. | 一氯甲烷 | B. | 溴乙烷 | C. | 1-氯丙烷 | D. | 邻氯甲苯 |
4.下列单质分子中,键长最长,键能最小的是( )
| A. | H2 | B. | Cl2 | C. | Br2 | D. | I2 |
11.利用下列反应不能制得括号中纯净物质的是( )
| A. | 乙烯与氯气加成(1,2-二氯乙烷) | |
| B. | 乙烯与水加成(乙醇) | |
| C. | 等物质的量的氯气与乙烷在光照条件下反应(一氯乙烷) | |
| D. | 液溴与苯用溴化铁作催化剂反应(溴苯) |
1.现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)已知B2A4是一种无色发烟的、具有腐蚀性和强还原性的无色油状液体,能很好地混溶于水,遇卤素、过氧化氢等强氧化剂作用能自燃.B2A4属于极性分子(填“极性”或“非极性”),B2A4分子中B原子轨道的杂化形式为sp3.写出B2A4的电子式: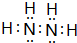 .
.
(2)B元素基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈哑铃形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 该同学所画的电子排布图违背了泡利原理.
该同学所画的电子排布图违背了泡利原理.
(4)分析DE3分子的空间构型为三角锥形.
(5)G位于第Ⅷ族d区,该元素的核外电子排布式为1s22s22p63s23p63d74s2.
(6)无水GE2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水GE2,故常在实验室中用作吸湿剂和空气湿度指示剂.
GE2+xH2O=GE2•xH2O
深蓝色 粉红色
现有65g无水GE2,吸水后变成GE2•xH2O 119g.
①水合物中x=6.
②若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-的个数比为1:1,则其化学式可表示为[CoCl(H2O)5]Cl•H2O.
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738kJ•mol-1 I2=1451kJ•mol-1 I3=7733kJ•mol-1 I4=10540kJ•mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中未成对电子最多的元素 |
| G的3d能级只含有2对成对电子 |
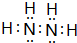 .
.(2)B元素基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈哑铃形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 该同学所画的电子排布图违背了泡利原理.
该同学所画的电子排布图违背了泡利原理.(4)分析DE3分子的空间构型为三角锥形.
(5)G位于第Ⅷ族d区,该元素的核外电子排布式为1s22s22p63s23p63d74s2.
(6)无水GE2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水GE2,故常在实验室中用作吸湿剂和空气湿度指示剂.
GE2+xH2O=GE2•xH2O
深蓝色 粉红色
现有65g无水GE2,吸水后变成GE2•xH2O 119g.
①水合物中x=6.
②若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-的个数比为1:1,则其化学式可表示为[CoCl(H2O)5]Cl•H2O.
5.明•于谦诗:“凿开混沌得乌金,藏蓄阳和意最深.爝火燃回春浩浩,洪炉照破夜沉沉.”这里“乌金”指的是( )
| A. | 煤 | B. | 磁铁矿 | C. | 石油 | D. | 金 |
6.用NA表示阿伏加德罗常数,下列有关说法正确的是( )
| A. | 2.0g D218O中含有的质子数为NA | |
| B. | 标准状况下,22.4L NH3分子含有的杂化轨道数为4NA | |
| C. | 78g Na2O2晶体中所含阴、阳离子个数均为2NA | |
| D. | 1mol Fe完全溶于一定量的硝酸溶液中,转移的电子数一定是3NA |
 水合肼(N2H4•H2O)为无色透明的油状液体,沸点为118.5℃,熔点为-40℃.具有强碱性,在空气中可吸收CO2,产生烟雾.水合肼是一种强还原剂,能与卤素单质、HNO3、KMnO4等激烈反应.水合肼可用含NaOH的NaClO溶液氧化尿索[CO(NH2)2]溶液制得.实验室模拟水合肼的制备装置如图所示(夹持及加热装置已省略).请回答下列问题:
水合肼(N2H4•H2O)为无色透明的油状液体,沸点为118.5℃,熔点为-40℃.具有强碱性,在空气中可吸收CO2,产生烟雾.水合肼是一种强还原剂,能与卤素单质、HNO3、KMnO4等激烈反应.水合肼可用含NaOH的NaClO溶液氧化尿索[CO(NH2)2]溶液制得.实验室模拟水合肼的制备装置如图所示(夹持及加热装置已省略).请回答下列问题: