题目内容
15.碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型髙效絮凝剂,在医药上也可于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的流程如图: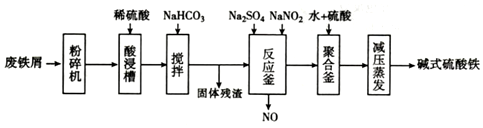
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)粉碎过筛的目的是选取细小颗粒,增大反应接触面积,提高“酸浸”反应速率.
(2)加入少量NaHCO3的目的是调节溶液pH,使溶液中的Al3+完全沉淀.
(3)反应釜中发生反应的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O.在实际生产中,常同时通入O2以减少NaNO2的用量,若参与反应的O2有11.2L(标准状况),则相当于约NaNO2的物质的量为2mol.
(4)聚合釜中溶液的pH必须控制在一定的范围内.pH偏小时Fe3+水解程度弱,PH偏大时则形成Fe(OH)3沉淀.
(5)相对于常压蒸发,减压蒸发的优点是减压蒸发,可防止温度过高,碱式硫酸铁分解.
分析 废铁屑中含少量氧化铝、氧化铁等,将过量废铁屑加入稀硫酸中,发生反应 Fe+H2SO4=FeSO4+H2↑、Al2O3+3H2SO4=Al2(SO4)3+3H2O、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O、Fe2(SO4)3+Fe=3FeSO4,然后反应I中加入NaHCO3并搅拌,调节溶液的pH,发生反应Al3++3HCO3-=Al(OH)3↓+3CO2↑,所以滤渣中成分是Al(OH)3,过滤得到硫酸亚铁,向硫酸亚铁溶液中加入稀硫酸和NaNO2,酸性条件下,NaNO2和FeSO4发生氧化还原反应生成铁离子、NO,将溶液蒸发浓缩、过滤得到碱式硫酸铁,
(1)固体溶解时,通过借助于固体粉碎、玻璃棒搅拌或加热等方法,加快固体溶解,提高浸取率;
(2)要制备硫酸亚铁,应与硫酸铝分离,需要调节溶液的pH在4.4≤pH<7.5之间;
(3)反应釜中发生的反应为Fe2+在酸性条件下被NO2-氧化为Fe3+,同时得到还原产物NO,可根据电子守恒和原子守恒写出此反应的离子方程式;
所消耗氧气得到的电子的物质的量相当于NaNO2得到电子的物质的量;
(4)Fe3+水解极易水解,pH过大易促进其水解生成Fe(OH)3沉淀,产物不纯;
(5)减压蒸发可以降低溶液的沸点.
解答 解:(1)为提高“酸浸”反应速率,可通过将固体粉碎过筛达到选取细小颗粒,增大反应接触面积来实现,故答案为:选取细小颗粒,增大反应接触面积,提高“酸浸”反应速率;
(2)为了使Fe3+和Al3+完全分离,可通过加入少量NaHCO3来调节溶液pH,使溶液中的Al3+完全沉淀,故答案为:调节溶液pH,使溶液中的Al3+完全沉淀;
(3)反应釜中Fe2+在酸性条件下被NO2-氧化为Fe3+,同时得到还原产物NO时发生反应的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O,n(O2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,则得到电子0.5mol×4=2mol,1mol NaNO2被还原生成NO,化合价由+3价降低到+2价,得到1mol电子,则需要2mol NaNO2,
故答案为:2H++Fe2++NO2-=Fe3++NO↑+H2O;2mol;
(4)为防止Fe3+水解生成Fe(OH)3沉淀,产物不纯,调节溶液pH时不易过大,故答案为:形成Fe(OH)3沉淀;
(5)蒸发时选择减压蒸发,可降低沸点,避免高温下碱式硫酸铁分解,故答案为:减压蒸发,可防止温度过高,碱式硫酸铁分解.
点评 本题考查制备原理的设计,题目难度中等,注意根据物质的性质和题给信息判断可能发生的反应,离子方程式的书写为解答该题的难点,也是易错点,注意体会书写方法.

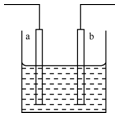
| A. | a,b可能是同种材料的电极 | |
| B. | 该装置可能是电解池,电解质溶液为稀硝酸 | |
| C. | 该装置可能是原电池,电解质溶液为稀盐酸 | |
| D. | 该装置可看作是铜一锌原电池,电解质溶液是稀硫酸 |
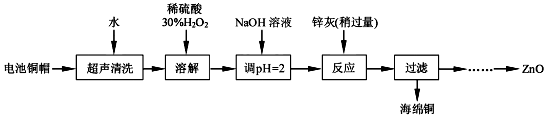
(1)①写出铜帽溶解过程中铜发生反应的化学方程式Cu+H2O2+H2SO4=CuSO4+2H2O.
②铜帽溶解后需将溶液中过量H2O2除去.除去H2O2的简便方法是加热(至沸腾).
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH至3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:
2Cu2++4I-=2CuI(白色)↓+I2 I2+2S2O32-=2I-+S4O62-
①滴定选用的指示剂为淀粉溶液,滴定终点观察到的现象为溶液蓝色褪去,且半分钟内不恢复.
②若滴定前溶液中H2O2没有除尽,所测得的Cu2+的含量将会偏高(填“偏高”、“偏低”、“不变”).
(3)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 完全沉淀的pH | 3.2 | 8.8 | 8.9 |
由回收铜后的滤液制备ZnO的实验步骤依次为:
①向滤液中加入略过量30%的H2O2,使其充分反应
②向反应后的溶液中滴加1.0moL•L-1的NaOH溶液,调节溶液的pH
范围为3.2~5.9;
③过滤;
④向滤液中滴加1.0moL•L-1的氢氧化钠,调节pH范围为8.9~11;
⑤过滤、洗涤、干燥
⑥900℃煅烧.
| 实验 编号 | 起始时各物质的物质的量/mol | 达到平衡时体系的变化 | 平衡时NH3的体积分数 | ||
| N2 | H2 | NH3 | |||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ | W1 |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q kJ | W2 |
| A. | W1>W2,Q<23.15 | B. | W1=W2,Q=23.15 | C. | W1<W2,Q>23.15 | D. | W1=W2,Q<23.15 |
| A. | 25℃、101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热 | |
| B. | 化石燃料在任何条件下都能充分燃烧 | |
| C. | 燃烧热或中和热是反应热的种类之一 | |
| D. | 弱酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
| A. | 直径介于1nm~100nm之间的微粒称为胶体 | |
| B. | 电泳现象可以证明胶体粒子带电 | |
| C. | 丁达尔效应是溶液与胶体的本质区别 | |
| D. | 胶体粒子很小,可以透过滤纸和半透膜 |
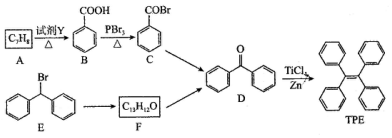
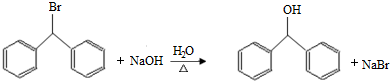 .
.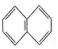 )的一元取代物;②存在羟甲基(-CH2OH).写出W所有可能的结构简式
)的一元取代物;②存在羟甲基(-CH2OH).写出W所有可能的结构简式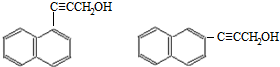 .
.