题目内容
12.向含有1.17g NaCl和1.17g NaF的溶液中,加入过量的AgNO3溶液,将析出的沉淀过滤、洗涤、干燥后称其质量为2.87g.根据此实验确定AgF在水中的溶解性应为( )| A. | 易溶于水 | B. | 此AgCl更难溶于水 | ||
| C. | 与AgCl一样难溶于水 | D. | 无法确定溶解性 |
分析 n(NaCl)=$\frac{1.17g}{58.5g/mol}$=0.02mol,加入过量的AgNO3溶液,将析出的沉淀过滤、洗涤、干燥后称其质量为2.87g,沉淀若为AgCl,n(AgCl)=$\frac{2.87g}{143.5g/mol}$=0.02mol,则n(NaCl)=n(AgCl),以此来解答.
解答 解:n(NaCl)=$\frac{1.17g}{58.5g/mol}$=0.02mol,加入过量的AgNO3溶液,将析出的沉淀过滤、洗涤、干燥后称其质量为2.87g,沉淀若为AgCl,n(AgCl)=$\frac{2.87g}{143.5g/mol}$=0.02mol,则n(NaCl)=n(AgCl),因硝酸银过量,可知AgF易溶于水,
故选A.
点评 本题考查难溶电解质,为高频考点,把握物质的量的计算、NaCl与沉淀的物质的量关系为解答的关键,侧重分析与计算能力的考查,注意氯离子守恒,题目难度不大.

练习册系列答案
相关题目
17.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 工业上电解熔融Al2O3制备金属铝 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | 金属锌与稀硫酸反应制取氢气,粗锌比纯锌反应速率快 | |
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
17.硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下,下列说法正确的是( )


| A. | 温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小 | |
| B. | 三个不同温度中,313K时Ksp(SrSO4)最小 | |
| C. | 283K时,图中a点对应的溶液是不饱和溶液 | |
| D. | 283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液 |
2.下列说法不正确的是( )
| A. | 2-乙基-1,3-丁二烯的键线式: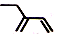 | |
| B. | 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等 | |
| C. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 | |
| D. | 用溴水可鉴别苯、CCl4、苯乙烯 |
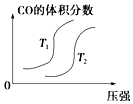
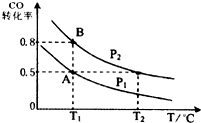 甲醇可作为燃料电池的原料.通过下列反应可以制备甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ•mol-1在一容积可变的密闭容器中充入10mol CO 和20mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20L.
甲醇可作为燃料电池的原料.通过下列反应可以制备甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ•mol-1在一容积可变的密闭容器中充入10mol CO 和20mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20L.