题目内容
NA为阿伏伽德罗常数.下列说法正确的是( )
| A、同温同压同体积的CO2和SO2所含氧原子数均为2NA |
| B、32gCu与S完全反应转移的电子数为NA |
| C、1L 1.0mol?L-1 NH4Cl与2L 0.5mol?L-1 NH4Cl溶液含NH4+数目相同 |
| D、25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.没有告诉二氧化碳和二氧化硫的物质的量,无法计算二者含有的氧原子数目;
B.铜与硫单质反应生成的是硫化亚铜,32g铜的物质的量为0.5mol,完全反应失去0.5mol电子;
C.铵根离子浓度不同,其水解程度不同,所以溶液中铵根离子数目不同;
D.pH=13的氢氧化钡溶液中氢氧根离子浓度为0.1mol/L,1L该溶液中含有0.1mol氢氧根离子.
B.铜与硫单质反应生成的是硫化亚铜,32g铜的物质的量为0.5mol,完全反应失去0.5mol电子;
C.铵根离子浓度不同,其水解程度不同,所以溶液中铵根离子数目不同;
D.pH=13的氢氧化钡溶液中氢氧根离子浓度为0.1mol/L,1L该溶液中含有0.1mol氢氧根离子.
解答:
解:A.缺少CO2和SO2的物质的量,无法计算含有的氧原子数目,故A错误;
B.32g铜的物质的量为0.5mol,0.5mol铜与硫单质完全反应生成0.25mol硫化亚铜,转移了0.5mol电子,转移的电子数为0.5NA,故B错误;
C.两溶液中都含有溶质氯化铵1mol,由于铵根离子浓度不同,铵根离子的水解程度不同,所以两溶液中铵根离子的物质的量及数目不相同,故C错误;
D.25℃时,pH=13的1.0L Ba(OH)2溶液中氢氧根离子浓度为0.1mol/L,1L该溶液中含有0.1mol氢氧根离子,含有的OH-数目为0.1NA,故D正确;
故选D.
B.32g铜的物质的量为0.5mol,0.5mol铜与硫单质完全反应生成0.25mol硫化亚铜,转移了0.5mol电子,转移的电子数为0.5NA,故B错误;
C.两溶液中都含有溶质氯化铵1mol,由于铵根离子浓度不同,铵根离子的水解程度不同,所以两溶液中铵根离子的物质的量及数目不相同,故C错误;
D.25℃时,pH=13的1.0L Ba(OH)2溶液中氢氧根离子浓度为0.1mol/L,1L该溶液中含有0.1mol氢氧根离子,含有的OH-数目为0.1NA,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项B为易错点,注意铜与硫反应的产物为硫化亚铜.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
下列离子方程式表达正确的是( )
| A、碘化亚铁溶液中通入少量氯气:Cl2+2Fe2+═2Fe3++2Cl- |
| B、向1mol/L 0.1L的明矾溶液中加入0.5mol/L 0.2L的Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
| C、将蛋壳浸泡到醋酸中:CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O |
| D、将过氧化钠与水反应:2O22-+2H2O═O2+4OH- |
对于反应aA+bB=dD+eE,该化学反应速率定义为v=
=
=
=
.式中v(X)指物质X=(X=A,B,D,E)的反应速率,a、b、d、e是化学计量数.298k时,测得溶液中的反应H2O2+2HI═2H2O+I2在不同浓度时化学反应速率v见下表:以下说法正确的是( )
| v(A) |
| a |
| v(B) |
| b |
| v(D) |
| d |
| v(E) |
| e |
| 实验编号 | 1 | 2 | 3 | 4 |
| c(HI)/mol?L-1 | 0.100 | 0.200 | 0.300 | 0.100 |
| c(H2O2)/mol?L-1 | 0.100 | 0.100 | 0.100 | 0.200 |
| v/mol?L-1?s-1 | 0.00760 | 0.0153 | 0.0227 | 0.0151 |
| A、实验1、2中,v(H2O2)相等 |
| B、将浓度均为0.200mol?L-1 H2O2和HI溶液等体积混合,反应开始时v=0.0304mol?L-1?s-1 |
| C、v与“HI和H2O2浓度的乘积”的比值为常数 |
| D、实验4,反应5秒后H2O2浓度减少了0.0755mol?L-1 |
常温下,pH=12的NaOH溶液和pH=2的醋酸混合后恰好完全反应(不考虑溶液体积的变化).下列说法正确的是( )
| A、反应后的溶液呈酸性 |
| B、两种反应物中水电离出的c(H+)都是1×10-12mol?L-1 |
| C、反应后的溶液中:c(CH3COO-)+c(CH3COOH)═0.01mol?L-1 |
| D、反应后的溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
下列实验装置或操作正确的是( )
A、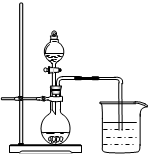 向Ⅰ中通入过量CO2,出现白色沉淀,则溶液中一定含有AlO2- |
B、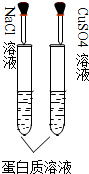 两支试管中蛋白质溶液均会变性 |
C、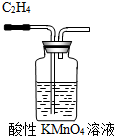 除去C2H4中的SO2 |
D、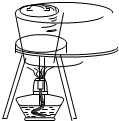 海带灼烧成灰 |
能达到实验目的是( )
A、 称NaOH固体的质量 |
B、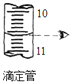 读数为10.60 |
C、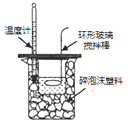 反应热的测定 |
D、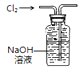 收集氯气 |
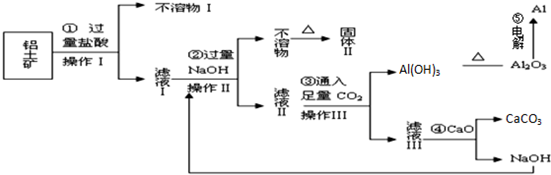
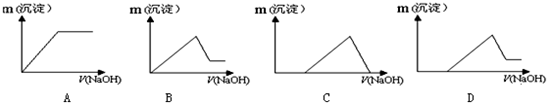
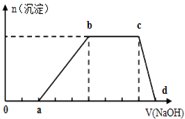 某溶液中可能含有H+、K+、NH4+、Mg2+、Fe3+、Al3+、Cu2+、SO42-、I-、CO32-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知:
某溶液中可能含有H+、K+、NH4+、Mg2+、Fe3+、Al3+、Cu2+、SO42-、I-、CO32-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知: