题目内容
某氯碱厂利用废铁皮制取净水剂FeCl3溶液,最合理的生产途径是( )
A、Cl2
| |||||||||
B、Cl2
| |||||||||
C、Cl2
| |||||||||
D、 |
考点:制备实验方案的设计,氯气的化学性质,铁盐和亚铁盐的相互转变
专题:元素及其化合物
分析:氢气与氯气在光照下可能发生爆炸,高温需要消耗能源,结合实验安全、能源消耗等来解答.
解答:
解:A.高温需要消耗能源,不适合制取净水剂FeCl3溶液,故A错误;
B.点燃下安静燃烧生成HCl,与Fe反应生成氯化亚铁,再氧化生成氯化铁,故B正确;
C.氢气和氯气光照容易发生爆炸,故C错误;
D.废铁高温生成氧化铁,消耗能源,不适合制取净水剂FeCl3溶液,故D错误;
故选B.
B.点燃下安静燃烧生成HCl,与Fe反应生成氯化亚铁,再氧化生成氯化铁,故B正确;
C.氢气和氯气光照容易发生爆炸,故C错误;
D.废铁高温生成氧化铁,消耗能源,不适合制取净水剂FeCl3溶液,故D错误;
故选B.
点评:本题考查氯气的性质及物质的制备,为高频考点,把握物质制备实验方案的评价、实验安全及能源等为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
硝酸汞和碘化钾溶液混合后会生成红色的碘化汞沉淀,为了探究硝酸汞和碘化钾溶液之间能否发生氧化还原反应,研究人员设计了如图的实验装置,结果电流计指针发生了偏转,下列分析正确的是( )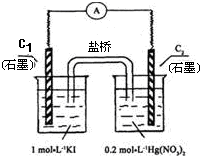

| A、C1电极上发生的反应是:2I--2e-=I2 |
| B、如图装置的电流方向是从C1到C2 |
| C、盐桥中的K+离子向C1电极移动 |
| D、装置发生的总反应是Hg2++2I-=HgI2↓ |
化学在生活中无处不在,其中不科学的是( )
| A、含食品添加剂的食品都不属于绿色食品 |
| B、维生素C具有还原性,在人体内起抗氧化作用 |
| C、为防止月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁 |
| D、地震后防疫人员在震区周围撒石灰,其作用是进行环境消毒,防止灾后出现疫情 |
可逆反应aA(?)+2B(g)?2C(g)+D(g),其中a为正整数.反应中当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )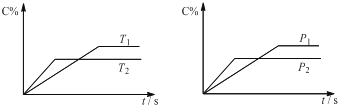

| A、达到平衡后,加入催化剂则C%增大 |
| B、达到平衡后,若升高温度,平衡正向移动 |
| C、a可以为任意的正整数 |
| D、达平衡后,增加A的量,有利于平衡正向移动 |
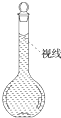 实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.