题目内容
19.试分析油脂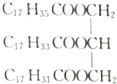 能发生的反应类型.若能反应,则1mol该油脂最多消耗溴的物质的量是多少?
能发生的反应类型.若能反应,则1mol该油脂最多消耗溴的物质的量是多少?
分析 油脂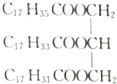 是由硬脂酸C17H35COOH、油酸C17H33COOH、亚油酸C17H31COOH和甘油形成的酯类,由于油酸C17H33COOH、亚油酸C17H31COOH均含碳碳双键,故油脂
是由硬脂酸C17H35COOH、油酸C17H33COOH、亚油酸C17H31COOH和甘油形成的酯类,由于油酸C17H33COOH、亚油酸C17H31COOH均含碳碳双键,故油脂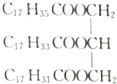 中含有的官能团为酯基和碳碳双键,据此分析能发生的反应和所消耗的溴.
中含有的官能团为酯基和碳碳双键,据此分析能发生的反应和所消耗的溴.
解答 解:油脂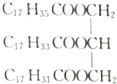 是由硬脂酸C17H35COOH、油酸C17H33COOH、亚油酸C17H31COOH和甘油形成的酯类,由于油酸C17H33COOH中含1条碳碳双键,亚油酸C17H31COOH中含2条碳碳双键,故油脂
是由硬脂酸C17H35COOH、油酸C17H33COOH、亚油酸C17H31COOH和甘油形成的酯类,由于油酸C17H33COOH中含1条碳碳双键,亚油酸C17H31COOH中含2条碳碳双键,故油脂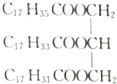 中含有的官能团为酯基和3条碳碳双键.
中含有的官能团为酯基和3条碳碳双键.
由于是有机物,故能燃烧;由于含酯基,故能发生水解;由于含碳碳双键,故能发生加成反应,还能使高锰酸钾溶液褪色,即发生氧化反应.
由于结构中含3条碳碳双键,故和溴水发生加成反应,则1mol此油脂能消耗3mol溴.
答:能发生水解反应、加成反应和氧化反应;1mol该油脂能消耗3mol溴.
点评 本题考查了油脂的结构和性质,难度不大,应注意的是根据有机物所含有的官能团来分析其所能发生的反应.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
9.聚合氯化铝(PAC)通式为[Al2(OH)nCl6-n]m,是无机高分子混凝剂,它是用软铝矿(主要成分Al2O3•H2O)为原料制备,制备的最后一步反应是将Al(OH)3凝胶与[Al(OH)2(H2O)4]Cl按照一定配比恰好完全反应制得PAC,则该反应中前者与后者的物质的量之比为( )
| A. | 1:1 | B. | $\frac{4-n}{6-n}$ | C. | $\frac{n-4}{6-n}$ | D. | $\frac{1}{m}$ |
10.下列说法错误的是( )
| A. | 金属的冶炼方法有4种,其中铝热反应属于热分解法 | |
| B. | 海带中碘元素的检验原理:2H++2I-+H2O2=I2+2H2O | |
| C. | 石油的分馏,裂化,裂解,催化重整中裂化是物理变化 | |
| D. | 铝热反应中铝做还原剂 |
7. 六种元素周期表中的位置如图,其中只有一种不是短周期元素,只有一种是金属元素,下列说法正确的是( )
六种元素周期表中的位置如图,其中只有一种不是短周期元素,只有一种是金属元素,下列说法正确的是( )
 六种元素周期表中的位置如图,其中只有一种不是短周期元素,只有一种是金属元素,下列说法正确的是( )
六种元素周期表中的位置如图,其中只有一种不是短周期元素,只有一种是金属元素,下列说法正确的是( )| A. | 简单离子半径大小:Q>Y>X | |
| B. | 最简单气态氢化物的沸点高低:Y>Z | |
| C. | Q的最高价氧化物可与X的氢化物直接反应 | |
| D. | X与Y既可存在于同一共价化合物中,也可存在于同一离子化合物中 |
14.下列各组化合物中,有关化学键类型的叙述正确的是( )
| A. | CaCl2中既含有离子键又含有共价键 | |
| B. | Na0H中既含有离子键又含有共价键 | |
| C. | Na2O2中只含有离子键 | |
| D. | 由非金属元素组成的物质NH4Cl中只有共价键 |
11.下列叙述正确的是( )
| A. | 苯中少量的苯酚可先加适量的浓溴水,使之生成三溴苯酚,再过滤除去 | |
| B. | 将苯酚晶体放入少量水中,加热时全部溶解,冷却后溶液仍澄清透明 | |
| C. | 苯酚的酸性很弱,不能使指示剂变色,但可以与NaCHO3反应放出CO2 | |
| D. | 苯酚有毒,但其稀溶液可直接用作防腐剂和消毒剂 |
12.下列说法正确的是( )
| A. | 原子最外层电子数为2的元素一定处于周期表ⅡA族 | |
| B. | 主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5 | |
| C. | 氯化氢的沸点比氟化氢的沸点高 | |
| D. | 第三周元素的离子半径从左到右逐渐减小 |
13.下列实验操作、现象和得出的结论均正确的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向某溶液中滴入几滴酸性KMnO4溶液,然后滴加KSCN溶液 | 溶液最终变为红色 | 原溶液中含有Fe3+ |
| B | 向浓度均为0.1mol•L-1NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | KSP(AgCl)>KSP(AgI) |
| C | 用洁净的铂丝蘸取某溶液,在酒精灯火焰上灼烧 | 透过蓝色钴玻璃观察到火焰颜色为紫色 | 原溶液中一定只含K+ |
| D | 在试管中取少量淀粉,加入稀硫酸后加热片刻,冷却后取澄清液滴入新制的Cu(OH)2加热煮沸 | 未见红色沉淀生成 | 淀粉未发生水解 |
| A. | A | B. | B | C. | C | D. | D |
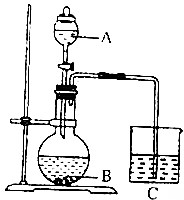 某化学小组设计如图装置完成一组实验;
某化学小组设计如图装置完成一组实验;