题目内容
17.能正确表示下列反应的离子方程式的是( )| A. | 将铁粉加入稀硫酸中:2Fe+6H+═Fe3++3H2↑ | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| C. | 将氯化亚铁溶液和稀硝酸混合:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| D. | 将铁屑加入Fe3+溶液中:Fe3++Fe═2Fe2+ |
分析 A.铁粉与稀硫酸反应生成硫酸亚铁和氢气;
B.四氧化三铁与盐酸反应生成亚铁离子和铁离子;
C.亚铁离子被稀硝酸氧化成铁离子;
D.离子方程式两边正电荷不相等,违反了电荷守恒.
解答 解:A.将铁粉加入稀硫酸中,反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故A错误;
B.将磁性氧化铁溶于盐酸,反应生成氯化亚铁和氯化铁,正确的离子方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O,故B错误;
C.将氯化亚铁溶液和稀硝酸混合,二者发生氧化还原反应,反应的离子方程式为:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑,故C正确;
D.将铁屑加入Fe3+溶液中,反应生成氯化亚铁,正确的离子方程式为:2Fe3++Fe═3Fe2+,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
相关题目
11.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
请回答下列问题:
(1)该反应的化学平衡常数表达式K=$\frac{c(CO)•c(H{\;}_{2}O)}{c(CO{\;}_{2})•c(H{\;}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”),升高温度,逆反应速率增大(填“增大”、“减小”或“不变”)
(3)温度不变,减小CO浓度,平衡向正反应方向移动(填“正反应”或“逆反应”),该反应平衡常数K 值不变(填“增大”、“减小”或“不变”)
(4)800℃时,固定容积的密闭容器中放入混合物,起始浓度为c(CO)=1mol•L-1,c(H2O)=3mol•L-1,c(CO2)=1mol•L-1,c(H2)=5mol•L-1,则反应开始时,H2O的消耗速率比生成速率小(填“大”、“小”或“不能确定”)
(5)t℃时,在2L的固定容积的密闭容器中放入4mol CO2和6mol H2,平衡后CO2的转化率为60%,则达到平衡时CO的体积分数为24%,反应温度t为830℃.
温度不变,若起始时投入3.6mol CO、3.6mol H2O和1.8mol H2,则达到平衡时CO的体积分数为24%,H2的平衡浓度为1.62mol/L.
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式K=$\frac{c(CO)•c(H{\;}_{2}O)}{c(CO{\;}_{2})•c(H{\;}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”),升高温度,逆反应速率增大(填“增大”、“减小”或“不变”)
(3)温度不变,减小CO浓度,平衡向正反应方向移动(填“正反应”或“逆反应”),该反应平衡常数K 值不变(填“增大”、“减小”或“不变”)
(4)800℃时,固定容积的密闭容器中放入混合物,起始浓度为c(CO)=1mol•L-1,c(H2O)=3mol•L-1,c(CO2)=1mol•L-1,c(H2)=5mol•L-1,则反应开始时,H2O的消耗速率比生成速率小(填“大”、“小”或“不能确定”)
(5)t℃时,在2L的固定容积的密闭容器中放入4mol CO2和6mol H2,平衡后CO2的转化率为60%,则达到平衡时CO的体积分数为24%,反应温度t为830℃.
温度不变,若起始时投入3.6mol CO、3.6mol H2O和1.8mol H2,则达到平衡时CO的体积分数为24%,H2的平衡浓度为1.62mol/L.
8.下列物质间的转化不可能通过一步反应实现的是( )
| A. | 铜→氧化铜 | B. | 氢氧化钙→氢氧化钠 | ||
| C. | 铜→碳酸铜 | D. | 碳酸钙→氯化钙 |
5.下列变化中,属于化学变化的是( )
| A. | 氯水光照后褪色 | B. | 溴挥发 | ||
| C. | 碘升华 | D. | 溴水加CCl4后溴水层褪色 |
2.下列说法中正确的是( )
| A. | 2CO2(g)═2CO(g)+O2(g)△H=+566.0 kJ•mol-1,则 CO(g)的燃烧热是-283.0kJ•mol-1 | |
| B. | H2SO4和NaOH反应的中和热△H=-57.3 kJ•mol-1,则1molH2SO4和1molBa(OH)2反应的反应热△H=-114.6kJ•mol-1 | |
| C. | 石墨转化为金刚石是吸热反应,可知金刚石的燃烧热更大 | |
| D. | 在恒温时,压缩容器的体积,则2SO2+O2?2SO3平衡正向移动,该反应的△H减小 |
9.短周期元素X、Y、Z、W、Q在周期表中的相对位置如图所示.下列说法不正确的是( )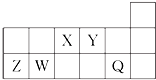

| A. | X与Y可以形成5种以上的化合物 | |
| B. | Y分别与Z、W形成的化合物的晶体类型相同 | |
| C. | 工业上常用电解法生产Z、Q的单质 | |
| D. | 简单气态氢化物的热稳定性:Y>X>W |
6.下列溶液中导电性最强的是( )
| A. | 1L 0.1mol/L醋酸 | B. | 0.5L 0.1mol/L H2SO4溶液 | ||
| C. | 1L 0.1mol/L盐酸 | D. | 2L 0.1mol/L H2SO3溶液 |
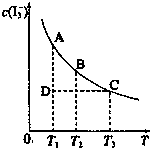 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I-3(aq).I2、KI混合溶液中,I-3的物质的量浓度c(I-3)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下到说法正确的组合是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I-3(aq).I2、KI混合溶液中,I-3的物质的量浓度c(I-3)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下到说法正确的组合是( )