题目内容
10.下列物质中,既含有极性共价键,又含有非极性共价键的是( )| A. | CH≡CH | B. | CO2 | C. | NH4Cl | D. | CH4 |
分析 不同非金属元素之间形成极性共价键,同种非金属元素之间形成非极性共价键,以此来解答.
解答 解:A.CH≡CH含C-H极性共价键和C-C非极性键,故A选;
B.CO2只含C-O极性键,故B不选;
C.NH4Cl只含N-H极性键,故C不选;
D.只含C-H极性共价键,故D不选;
故选A.
点评 本题考查共价键及类型,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
20.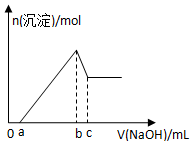 某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、Cl-、SO42-、NO3-中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加入NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )
某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、Cl-、SO42-、NO3-中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加入NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )
 某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、Cl-、SO42-、NO3-中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加入NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )
某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、Cl-、SO42-、NO3-中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加入NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )| A. | 一定没有NO3- | B. | 可能有K+、NO3-、SO42- | ||
| C. | 不能确定是否含有K+、NO3- | D. | 一定有Mg2+、Al3+、Cl-、SO42- |
1.下列化学方程式或离子方程式正确的是( )
| A. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu↓+O2↑+4H+ | |
| B. | 惰性电极电解MgCl2溶液:Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$OH-+Cl2↑+H2↑ | |
| C. | 乙醛溶液中加入新制碱性Cu(OH)2悬浊液并加热CH3CHO+2 Cu(OH)2+OH-$\stackrel{△}{→}$ CH3COO-+Cu2O↓+3H2O | |
| D. | 硝酸银溶液中滴加过量氨水:Ag++NH3•H2O═AgOH↓+NH${\;}_{4}^{+}$ |
5.下列关于化学键的说法不正确的是( )
| A. | 化学键存在于分子之间 | |
| B. | 化学键存在于分子内部 | |
| C. | 化学键是一种作用力 | |
| D. | 化学键可以是原子间作用力,也可以是离子间作用力 |
15.下列离子方程式正确的是( )
| A. | 向氨水通入足量SO2:SO2+2NH3•H2O═2NH4++SO32-+H2O | |
| B. | 将Ba(OH)2溶液滴入NaHSO4溶液中至SO42-恰好完全沉淀:Ba2++SO42-+2OH-+2H+═BaSO4↓+2H20 | |
| C. | 向醋酸溶液中滴加过量NaOH溶液:H++OH-═H2O | |
| D. | 向新制Cu(OH)2悬浊液中加入乙醛溶液并加热:CH3CHO+2Cu(OH)2+OH-$\stackrel{加热}{→}$ CH3COO-+Cu2O↓+3H2O |
2.类比推理是常用的思维方法,下列几种类比推理正确的是( )
| A. | CO2是直线型分子,推测CS2是直线型分子 | |
| B. | Cl?与Fe3+共存,推测I?与Fe3+共存 | |
| C. | H2SO4为强酸,推测HC1O为强酸 | |
| D. | 蒸干Al2(SO4)3溶液得到Al2(SO4)3固体,推测蒸干AlCl3溶液得到AlCl3固体 |
19.下列反应可用离子方程式“H++OH-=H2O”表示的是( )
| A. | NaHSO4溶液与Ba(OH)2溶液混合 | B. | 氢氧化镁溶于盐酸 | ||
| C. | 澄清石灰水与硝酸混合 | D. | 醋酸除去水垢 |
4.下列物质中含有共价键的、离子键的离子化合物是( )
| A. | H2O | B. | CaCl2 | C. | Ba(OH)2 | D. | H2 |