题目内容
8.如图所示,通电后A极上析出Ag,对该装置的有关叙述正确的是( )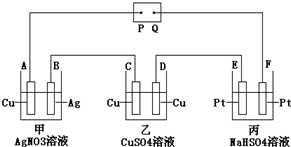
| A. | P是电源的正极 | |
| B. | F极上发生的反应为:4OH--4e-=2H2O+O2↑ | |
| C. | 电解时,甲、乙、丙三池中,除E、F两极外,其余电极均参加了反应 | |
| D. | 通电后,甲池溶液的pH减小,乙池溶液的浓度增大、丙池溶液的pH不变 |
分析 电解池中,有金属析出的电极是阴极,据此确定电解池的各个电极名称以及电源名称,在电解池的阳极上发红色呢过失电子的氧化反应,阴极上发生得电子的还原反应,根据电极反应以及电子转移知识来计算回答.
解答 解:该电解池中,有金属析出的电极A极是阴极,所以B是阳极,C是阴极,D是阳极,E是阴极,F是阳极,Q是正极,P是负极;
A、P是电源的负极,故A错误;
B、F极是阳极,电解硫酸氢钠溶液,根据放电顺序,该电极上发生的反应为:4OH--4e-=2H2O+O2↑,故B正确;
C、在电解池中,阳极上是活泼电极时,则该电极上是电极本身失电子的反应,所以电极B、D的电极参加了反应,其余的没有,故C错误;
D、甲池是电镀池原理液,所以pH不变,电解硫酸铜溶液,两极上放电的微粒让溶液中的铜离子浓度不变,pH不变,电解硫酸钠,实质是电解水所以酸性增大,pH减小,故D错误.
故选B.
点评 本题考查学生电解池的工作原理的应用以及电极反应式的书写知识,注意知识的应用是关键,难度不大.

练习册系列答案
相关题目
18.波立维是国家引进的药,它给中风、心肌梗死等心脏病患者带来福音.波立维属于硫酸氢盐,它的结构如图所示.下列关于它的说法正确的是( )
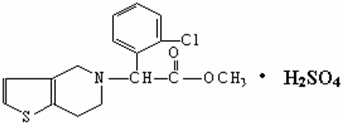

| A. | 该物质的化学式为C16H15ClNO2•H2SO4 | |
| B. | 该物质不溶于水 | |
| C. | 波立维能和氢气反应,每摩最多可消耗3mol氢气 | |
| D. | 它可以与NaOH溶液反应,1mol该物质最多可消耗5molNaOH |
19.下列反应起了氮的固定作用是( )
| A. | N2和H2在一定条件下反应生成NH3 | |
| B. | NH3经过一系列反应之后生成硝酸盐 | |
| C. | NO与O2反应生成NO2 | |
| D. | 氯化铵受热分解 |
16.下列物质一定属于同系物的是( )
①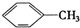 ②
②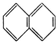 ③
③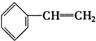 ④C2H4
④C2H4
⑤CH2═CH-CH═CH2 ⑥C3H6 ⑦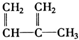 ⑧
⑧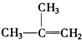
①
 ②
② ③
③ ④C2H4
④C2H4⑤CH2═CH-CH═CH2 ⑥C3H6 ⑦
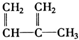 ⑧
⑧
| A. | ①和② | B. | ④和⑥ | C. | ④和⑧ | D. | ⑦和⑧ |
3.某元素X,其原子的电子层数为(n-1),最外层电子数为(2n-1).下列有关元素X的说法中正确的是( )
| A. | X可能是金属元素 | |
| B. | 由X形成的含氧酸均为强酸 | |
| C. | X不能形成化学式为KXO4的含氧酸盐 | |
| D. | 元素X的气态氢化物一定极易溶于水 |
20.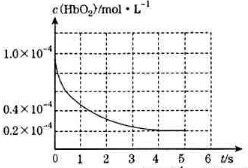 人体吸入CO后在肺部发生反应CO+HbO2?O2+HbCO导致人体缺氧.向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L]氧合血红蛋白HbO2浓度随时间变化曲线如图所示,下列说法正确的是( )
人体吸入CO后在肺部发生反应CO+HbO2?O2+HbCO导致人体缺氧.向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L]氧合血红蛋白HbO2浓度随时间变化曲线如图所示,下列说法正确的是( )
 人体吸入CO后在肺部发生反应CO+HbO2?O2+HbCO导致人体缺氧.向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L]氧合血红蛋白HbO2浓度随时间变化曲线如图所示,下列说法正确的是( )
人体吸入CO后在肺部发生反应CO+HbO2?O2+HbCO导致人体缺氧.向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L]氧合血红蛋白HbO2浓度随时间变化曲线如图所示,下列说法正确的是( )| A. | 反应开始至4s内用HbO2表示的平均反应速率为2×10-4mol/(L•s) | |
| B. | 反应达平衡之前,O2与HbO2的反应速率逐渐减小 | |
| C. | 将CO中毒病人放入高压氧舱治疗是利用了化学平衡移动原理 | |
| D. | 该温度下反应CO+HbO2?O2+HbCO的平衡常数为107 |
7.甲、乙两个研究性学习小组拟从实验室含碘废液中回收碘.制订两种方案提取,他们的实验方案如下:
(甲小组实施的为方案一,乙小组实施的为方案二)
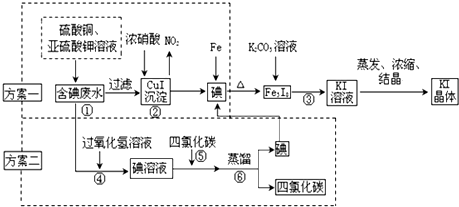
I.CuI在酸性介质中采用FeCl3氧化成即可生成单质碘.请写出上述化学反应方程式2CuI+4Fe3+═4Fe2++2Cu2++I2↓.
Ⅱ.蒸馏时用到的玻璃仪器,除接受器、锥形瓶、酒精灯外,还缺少的玻璃仪器有蒸馏烧瓶、冷凝器、温度计.
Ⅲ.甲小组为测定含碘废水中碘的含量.进行了以下实验操作:
A.各取1000g实验室废水,进行以上操作后,将所得KI晶体溶于适量水中配置成100mL溶液;
B.取KI溶液20mL于锥形瓶中;
C.用稀硫酸酸化所得KI溶液,加入足量KIO3溶液,使KIO3与KI反应完全;
D.以淀粉为指示剂,逐滴加入物质的量浓度为0.3mol•L-1的Na2S2O3溶液20.0mL,恰好反应完全.
已知:I2+2S2O32-=2I-+S4O62-;
(1)请写出步骤 C 中的离子反应方程式.5I-+IO3-+6H+=3I2↓+3H2O
(2)该废液中碘的质量分数为0.32%.
Ⅳ.(1)步骤③中的操作名称为过滤,通过该步操作还得到另一黑色固体物质.
(2)乙小组同学针对该黑色物质的成分,进行了如下步骤进行定性分析:
①在进行步骤四前是否要滴加指示剂?否(填“是”或“否”),请说明理由KMnO4溶液自身可作指示剂.
②通过以上步骤进行分析,该黑色物质可能为Fe3O4.
(甲小组实施的为方案一,乙小组实施的为方案二)

I.CuI在酸性介质中采用FeCl3氧化成即可生成单质碘.请写出上述化学反应方程式2CuI+4Fe3+═4Fe2++2Cu2++I2↓.
Ⅱ.蒸馏时用到的玻璃仪器,除接受器、锥形瓶、酒精灯外,还缺少的玻璃仪器有蒸馏烧瓶、冷凝器、温度计.
Ⅲ.甲小组为测定含碘废水中碘的含量.进行了以下实验操作:
A.各取1000g实验室废水,进行以上操作后,将所得KI晶体溶于适量水中配置成100mL溶液;
B.取KI溶液20mL于锥形瓶中;
C.用稀硫酸酸化所得KI溶液,加入足量KIO3溶液,使KIO3与KI反应完全;
D.以淀粉为指示剂,逐滴加入物质的量浓度为0.3mol•L-1的Na2S2O3溶液20.0mL,恰好反应完全.
已知:I2+2S2O32-=2I-+S4O62-;
(1)请写出步骤 C 中的离子反应方程式.5I-+IO3-+6H+=3I2↓+3H2O
(2)该废液中碘的质量分数为0.32%.
Ⅳ.(1)步骤③中的操作名称为过滤,通过该步操作还得到另一黑色固体物质.
(2)乙小组同学针对该黑色物质的成分,进行了如下步骤进行定性分析:
| 步骤 | 操作 | 现象 |
| 一 | 取黑色物质于烧杯中,加适量水进行洗涤、干燥 | 黑色物质未溶解 |
| 二 | 取适量固体于稀硫酸中进行充分溶解 | 无气体生成 |
| 三 | 移取少量步骤二溶液于试管A中,并滴加硫氰化钾溶液 | 溶液为血红色 |
| 四 | 移取少量步骤二溶液于试管B中,滴加酸性KMnO4溶液 | 酸性KMnO4溶液褪色 |
②通过以上步骤进行分析,该黑色物质可能为Fe3O4.