题目内容
10.普通汽油是由多种烃组成的混合物,乙醇汽油是用普通汽油与乙醇按照一定比例调和而成.下列说法正确的是( )| A. | 乙醇汽油是纯净物 | B. | 乙醇汽油易溶于水 | ||
| C. | 乙醇易溶于水 | D. | 汽油和乙醇都含有氧元素 |
分析 A.纯净物只含一种物质;
B.乙醇汽油中的汽油为烃混合物,不溶于水;
C.依据乙醇的水溶性解答;
D.汽油为烃的混合物.
解答 解:A.依据题意:乙醇汽油是用普通汽油与乙醇按照一定比例调和而成,属于混合物,故A错误;
B.乙醇汽油中的汽油为烃混合物,不溶于水,故B错误;
C.乙醇易溶于水,能够与水以任意比混溶,故C正确;
D.汽油为烃的混合物,不含有氧,故D错误;
故选:C.
点评 本题主要考查学生对车用乙醇汽油和乙醇的性质,熟悉乙醇和汽油的成分是解题关键,题目难度不大.

练习册系列答案
相关题目
20.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O═CH3COOH+4H+.下列有关说法正确的是( )
| A. | 检测时,电解质溶液中的H+向负极移动 | |
| B. | 若有0.2mol电子转移,则消耗2.24L氧气 | |
| C. | 电池反应的化学方程式为:CH3CH2OH+O2═CH3COOH+H2O | |
| D. | 正极上发生的反应是:O2+4e-+2H2O═4OH- |
1.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
(1)过氧化氢分解的化学方程式为2H2O2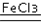 2H2O+O2↑.
2H2O+O2↑.
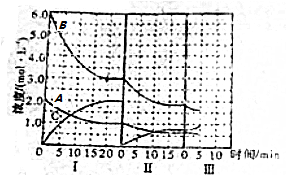
(2)实验①的目的是研究温度对H2O2分解速率的影响.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率 (用实验中提供的试剂).
(4)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:
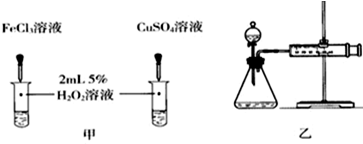
①定性分析:如图甲可通过观察溶液中气泡产生的速率,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是控制阴离子相同,排除阴离子的干扰.
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴等浓度 FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. | 试管A中不再产生气泡;试管B中产生的气泡量增大. |
| ② | 另取两支试管分别加入5mL 5% H2O2溶液和5mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生. |
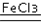 2H2O+O2↑.
2H2O+O2↑.(2)实验①的目的是研究温度对H2O2分解速率的影响.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率 (用实验中提供的试剂).
(4)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:

①定性分析:如图甲可通过观察溶液中气泡产生的速率,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是控制阴离子相同,排除阴离子的干扰.
5.下列有关化学反应速率和化学平衡的说法正确的是( )
| A. | 可逆反应达到化学平衡状态时,正、逆反应速率均等于零 | |
| B. | 当反应物与生成物浓度相等时,可逆反应一定已达到化学平衡 | |
| C. | 化学反应的限度决定了反应物在该条件下的最大转化率 | |
| D. | 镀锌铁制品镀层受损后,铁制品比受损前更易生锈 |
15.分子式为C3H4ClBr链状有机物的同分异构体共有(不考虑顺反异构)( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
2.下列属于苯的同系物的是( )
| A. | 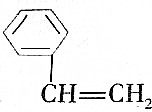 | B. | 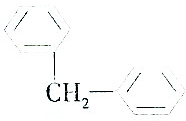 | ||
| C. | 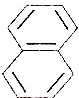 | D. | 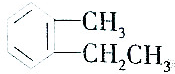 |
9.下列化学用语的书写正确的是( )
| A. | 氯原子的结构示意图为  | |
| B. | 质量数为37的氯原子${\;}_{17}^{37}$Cl | |
| C. | 氯化镁的电子式:Mg2+[Cl]2 | |
| D. | 用电子式表示氯化氢分子的形成过程: |