题目内容
我国是镁资源最为丰富的国家之一.
(1)将1mol镁铝合金(Mg17Al12)完全溶解于12L 6mol/L的盐酸中,放出氢气 mol,为使反应后溶液中的Mg2+、Al3+完全沉淀,需加入10mol/L的氨水至少 L.
(2)灼烧碱式碳酸镁可得到MgO.取碱式碳酸镁4.66g,灼烧至恒重,得到2g固体和1.76g CO2,某学生为确定碱式碳酸镁的化学式列了以下联立方程:
24+17x+60y+18z=4.66÷(
)…①
2-x-2y=0…②
(
)×(0.5x+z)×18=4.66-2-1.76…③
(a)①式表达的是求算碱式碳酸镁摩尔质量的关系式,则②式表达的是 ;
(b)以上关系式是正确的,据此可求出该碱式碳酸镁的化学式为 .
(3)氧化镁可用于烟气脱硫,反应原理为:
MgO+H2O→Mg(OH)2 Mg(OH)2+SO2→MgSO3+H2O
MgSO3+H2O+SO2→Mg(HSO3)2 2MgSO3+O2→2MgSO4
某小组模拟脱硫过程如下(实验在25℃进行):将MgO加入水中,不断搅拌,通入SO2和空气,得到550g滤液和若干克滤渣.取55g滤液依次加入足量的盐酸和BaCl2溶液,得到0.897g白色沉淀;另取55g滤液加入足量氯水和BaCl2混合溶液,得到1.992g白色沉淀.分析知滤渣中含MgSO3 16.82g(其它成分不含硫元素).
(1)该实验过程中吸收的SO2的物质的量为 mol;消耗氧气的物质的量为 mol.
(2)Mg(HSO3)2易溶于水;25℃溶解度,MgSO4:33.7g/100g水;MgSO3:0.652g/100g水.试通过计算确定550g滤液中镁盐的成分及物质的量(写出计算过程).
(1)将1mol镁铝合金(Mg17Al12)完全溶解于12L 6mol/L的盐酸中,放出氢气
(2)灼烧碱式碳酸镁可得到MgO.取碱式碳酸镁4.66g,灼烧至恒重,得到2g固体和1.76g CO2,某学生为确定碱式碳酸镁的化学式列了以下联立方程:
24+17x+60y+18z=4.66÷(
| 2 |
| 40 |
2-x-2y=0…②
(
| 2 |
| 40 |
(a)①式表达的是求算碱式碳酸镁摩尔质量的关系式,则②式表达的是
(b)以上关系式是正确的,据此可求出该碱式碳酸镁的化学式为
(3)氧化镁可用于烟气脱硫,反应原理为:
MgO+H2O→Mg(OH)2 Mg(OH)2+SO2→MgSO3+H2O
MgSO3+H2O+SO2→Mg(HSO3)2 2MgSO3+O2→2MgSO4
某小组模拟脱硫过程如下(实验在25℃进行):将MgO加入水中,不断搅拌,通入SO2和空气,得到550g滤液和若干克滤渣.取55g滤液依次加入足量的盐酸和BaCl2溶液,得到0.897g白色沉淀;另取55g滤液加入足量氯水和BaCl2混合溶液,得到1.992g白色沉淀.分析知滤渣中含MgSO3 16.82g(其它成分不含硫元素).
(1)该实验过程中吸收的SO2的物质的量为
(2)Mg(HSO3)2易溶于水;25℃溶解度,MgSO4:33.7g/100g水;MgSO3:0.652g/100g水.试通过计算确定550g滤液中镁盐的成分及物质的量(写出计算过程).
考点:化学方程式的有关计算
专题:计算题
分析:(1)n(HCl)=12L×6mol/L=72mol,Mg~2HCl、Al~3HCl,以此计算生成的氢气;酸碱恰好中和时Mg2+、Al3+完全沉淀;
(2)(a)②式与化合物中正负化合价代数和为0有关;
(b)以上关系式是正确的,联立方程计算x、y、z,可得碱式碳酸镁的化学式;
(3)0.897g白色沉淀为硫酸钡;另取55g滤液加入足量氯水和BaCl2混合溶液,得到1.992g白色沉淀为硫酸钡,滤渣中含MgSO3 16.82g,结合硫原子守恒计算二氧化硫的物质的量,结合电子守恒计算氧气的量;确定550g滤液中镁盐的成分为Mg(HSO3)2,结合上述反应及守恒计算.
(2)(a)②式与化合物中正负化合价代数和为0有关;
(b)以上关系式是正确的,联立方程计算x、y、z,可得碱式碳酸镁的化学式;
(3)0.897g白色沉淀为硫酸钡;另取55g滤液加入足量氯水和BaCl2混合溶液,得到1.992g白色沉淀为硫酸钡,滤渣中含MgSO3 16.82g,结合硫原子守恒计算二氧化硫的物质的量,结合电子守恒计算氧气的量;确定550g滤液中镁盐的成分为Mg(HSO3)2,结合上述反应及守恒计算.
解答:
解:(1)n(HCl)=12L×6mol/L=72mol,Mg~2HCl、Al~3HCl,1mol镁铝合金(Mg17Al12)消耗HCl为17mol×2+12mol×3=70,生成的氢气为
=35mol;酸碱恰好中和时Mg2+、Al3+完全沉淀,则需加入10mol/L的氨水至少
=7.2L,
故答案为:35;7.2;
(2)(a)②式与化合物中正负化合价代数和为0有关,即2-x-2y=0表达的是电荷平衡(或化合物化合价代数和为零),
故答案为:电荷平衡(或化合物化合价代数和为零);
(b)24+17x+60y+18z=4.66÷(
)…①
2-x-2y=0…②
(
)×(0.5x+z)×18=4.66-2-1.76…③
x表示OH-个数,y表示碳酸根离子个数,z表示水分子个数,以上关系式是正确的,联立方程可得Mg、x、y、z的个数比为5:2:4:4,
所以碱式碳酸镁的化学式为Mg(OH)2?4MgCO3?4H2O 或Mg5(OH)2(CO3)4?4H2O或Mg(OH)0.4(CO3)0.8?0.8H2O,
故答案为:Mg(OH)2?4MgCO3?4H2O 或Mg5(OH)2(CO3)4?4H2O或Mg(OH)0.4(CO3)0.8?0.8H2O;
(3)0.897g白色沉淀为硫酸钡;另取55g滤液加入足量氯水和BaCl2混合溶液,得到1.992g白色沉淀为硫酸钡,滤渣中含MgSO3 16.82g,
①由S原子守恒可知,n(SO2)=
+
=0.247mol,
由生成0.897g沉淀时电子守恒可知n(O2)=
=0.0192 mol,
故答案为:0.247;0.0192;
②MgSO3不溶于水,硫酸根离子转化为沉淀,则550g滤液中镁盐的成分为Mg(HSO3)2,
n(MgSO4)=
=0.0384mol,
m(MgSO3)=550g×
=3.563g,
n(MgSO3)=
=0.0343mol,
则由Mg(HSO3)2 产生的n(BaSO4)=
-0.0384mol-0.0352mol=0.0127mol,
所以n[Mg(HSO3)2]=
=0.00635mol,
答:550g滤液中镁盐的成分为Mg(HSO3)2,物质的量为0.00635mol.
| 70mol |
| 2 |
| 72mol |
| 10mol/L |
故答案为:35;7.2;
(2)(a)②式与化合物中正负化合价代数和为0有关,即2-x-2y=0表达的是电荷平衡(或化合物化合价代数和为零),
故答案为:电荷平衡(或化合物化合价代数和为零);
(b)24+17x+60y+18z=4.66÷(
| 2 |
| 40 |
2-x-2y=0…②
(
| 2 |
| 40 |
x表示OH-个数,y表示碳酸根离子个数,z表示水分子个数,以上关系式是正确的,联立方程可得Mg、x、y、z的个数比为5:2:4:4,
所以碱式碳酸镁的化学式为Mg(OH)2?4MgCO3?4H2O 或Mg5(OH)2(CO3)4?4H2O或Mg(OH)0.4(CO3)0.8?0.8H2O,
故答案为:Mg(OH)2?4MgCO3?4H2O 或Mg5(OH)2(CO3)4?4H2O或Mg(OH)0.4(CO3)0.8?0.8H2O;
(3)0.897g白色沉淀为硫酸钡;另取55g滤液加入足量氯水和BaCl2混合溶液,得到1.992g白色沉淀为硫酸钡,滤渣中含MgSO3 16.82g,
①由S原子守恒可知,n(SO2)=
| 1.992g×10 |
| 233g/mol |
| 16.82g |
| 104g/mol |
由生成0.897g沉淀时电子守恒可知n(O2)=
| ||
| 2 |
故答案为:0.247;0.0192;
②MgSO3不溶于水,硫酸根离子转化为沉淀,则550g滤液中镁盐的成分为Mg(HSO3)2,
n(MgSO4)=
| 0.897g×10 |
| 233g/mol |
m(MgSO3)=550g×
| 0.652g |
| 100g+0.652g |
n(MgSO3)=
| 3.563g |
| 104g/mol |
则由Mg(HSO3)2 产生的n(BaSO4)=
| 1.992g×10 |
| 233g/mol |
所以n[Mg(HSO3)2]=
| 0.0127mol |
| 2 |
答:550g滤液中镁盐的成分为Mg(HSO3)2,物质的量为0.00635mol.
点评:本题考查化学反应方程式的计算,为高频考点,把握发生的化学反应及守恒法计算为解答的关键,侧重分析能力、计算能力的考查,综合性较强,题目难度较大.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
下列实验装置能达到实验目的是( )
A、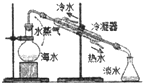 海水蒸馏 |
B、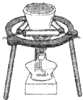 钾在空气中的燃烧 |
C、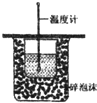 测定中和热 |
D、 牺牲阳极的阴极保护法 |
在下列各溶液中,离子一定能大量共存的是( )
| A、能与铝反应放出氢气的溶液中:K+、Al3+、Cl-、SO42- |
| B、水电离出来的c(H+)=10-12mol/L的溶液 Na+、Cl-、Br-、Ba2+ |
| C、所含溶质为Na2SO4的溶液 K+、CO32-、NO3-、Al3+ |
| D、室温下,pH=1的无色溶液中:Na+、Fe3+、NO3-、SO42- |
化学无处不在,下列与化学有关的说法正确的是( )
| A、液氨汽化时能吸收大量的热,故可用作制冷剂 |
| B、SO2能漂白纸浆等,故可广泛用于食品的漂白 |
| C、味精的主要成分是蛋白质,烧菜时可加入适量 |
| D、氢氟酸可用于雕刻玻璃制品,这是利用酸的通性 |
下列表述正确的是( )
| A、由水电离出的c(H+)=10-13mol?L-1的溶液中,Na+、NO3-、SO42-、Cl-一定能大量共存 |
| B、与强酸、强碱都能反应的物质种类只有两性氧化物或两性氧氧化物 |
| C、在NaHS溶液中存在的电离有:NaHS=Na++HS-,HS-?H++S2-,H2O?H++OH-,S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH- |
| D、若酸性HA>HB,则等物质的量浓度等体积的NaA和NaB溶液混合后,离子浓度关系为:c(OH-)>c(B-)>c(A-)>c(H+) |
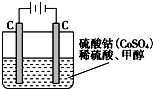
 )是一种化学活性很高的烃,存在于煤焦油中.
)是一种化学活性很高的烃,存在于煤焦油中.