题目内容
17.某研宄性小组借助A-D的仪器装置完成有关实验.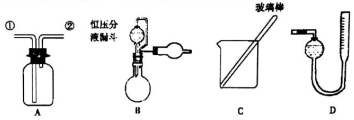
为了探究镀锌薄铁板上的锌的质量分数w (Zn)和镀层厚度,査询得知锌易溶于强碱; Zn+2NaOH=NaZnO2+H2↑.据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为mlg.用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验.
方案甲:通过测量试样与碱反应生成的氢气体积来实现探究目标.
(1)选用B和D(填仪器标号)两个装置进行实验.
(2)测得充分反应后生成氢气的体枳为VL(标准状况),w (Zn)=$\frac{65V}{22.4m{\;}_{1}}$.
(3)计算镀层厚度,还需要检索的一个物理量是金属锌的密度.
(4)若装置B中的恒压分液漏斗改为普通分液漏,测量结果将偏大(填“偏大”、“偏小”或“无影响”).方案乙,通过称量试样与碱反应前后的质量实现探究目标.选用仪器做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2g.
(5)w(Zn)=$\frac{m{\;}_{1}-m{\;}_{2}}{m{\;}_{1}}$.
(6)从实验误差度分析,方案丙劣于方案乙(“优于”、“劣于”或“等同于”).
分析 (1)Zn和Fe中只有Zn可以与NaOH产生气体,通过排水收集气体,根据反应方程式即可算出Zn的质量分数;
(2)计算生成氢气的物质的量,根据电子守恒计算Zn的质量,进而计算Zn的质量分数;
(3)可以获得Zn的质量,如果有密度,则可以求出Zn的体积,再由Zn的截面积可求出Zn的厚度;
(4)若装置B中的恒压分液漏斗改为普通分液漏斗,加入氢氧化钠溶液排出空气体积会计算在生成氢气的体积之内;
(5)锌与氢氧化钠反应溶解,铁与氢氧化钠不反应,所以固体减少的质量为锌的质量,据此解答;
(6)实验中产生氢气的量较少,测量氢气质量带来的误差更大.
解答 解:(1)Zn和Fe中只有Zn可以与NaOH产生气体,通过排水收集气体,根据反应方程式即可算出Zn的质量分数,所以需要的装置有测H2的体积的D装置,
故答案为:D;
(2)根据电子转移守恒,可知n(Zn)=n(H2)=$\frac{VL}{22.4L/mol}$=$\frac{V}{22.4}$mol,则w (Zn)=$\frac{\frac{V}{22.4}×65}{m{\;}_{1}}$=$\frac{65V}{22.4m{\;}_{1}}$,故答案为:$\frac{65V}{22.4m{\;}_{1}}$;
(3)有可以获得Zn的质量,如果有密度,则可以求出Zn的体积,再由Zn的截面积可求出Zn的厚度,
故答案为:金属锌的密度;
(4)恒压式分液漏斗产生的气体有部分残留在分液漏斗上方,故排气时收集少了,所以用普通漏斗时收集的H2多一些,则计算出的Zn的量偏大;
故答案为:偏大;
(5)锌与氢氧化钠反应溶解,铁与氢氧化钠不反应,所以固体减少的质量为锌的质量,则锌的质量分数为:$\frac{m{\;}_{1}-m{\;}_{2}}{m{\;}_{1}}$;
故答案为:$\frac{m{\;}_{1}-m{\;}_{2}}{m{\;}_{1}}$;
(6)丙方案根据H2的质量差值,显然误差大,因为产生的H2质量很小,计算偏差大;
故答案为:劣于.
点评 本题考查物质含量测定,关键是测定原理的理解,侧重考查学生分析问题、设计实验的能力,注意定量实验中尽可能的减少误差.

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案| A. | 摩尔质量为17 g•mol-1 | |
| B. | 所含的分子数目约为9.03×1023 | |
| C. | 在标准状况下体积约为33.6L | |
| D. | 溶于水制成0.5L溶液时物质的量浓度为1.5mol•L-1 |
下列实验操作、现象和结论均正确的是( )
选项 | 实验操作 | 现象 | 结 |
A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
B | 向稀的苯酚水溶液中滴加饱和溴水 | 生成白色沉淀 | 产物三溴苯酚不溶于水 |
C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 还原性:Cl- > I- |
D | 向FeSO4溶液中先滴入KSCN溶液再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+既有氧化性又有还原性 |
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 1.80 | 1.64 | 1.52 | 1.44 | 1.40 | 1.40 |
(2)不能说明该反应达到化学平衡状态的是BC.
A.正、逆反应速率相等
B.c(HI):c(H2):c(I2)=2:1:1
C.反应容器内气体的总物质的量不随时间变化
II.回答下列问题:
(3)葡萄糖在酒化酶的作用下可以得到乙醇.乙醇与乙酸反应生成有香味的产物,该反应的化学方程式为CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,反应类型为取代反应(或酯化反应).
(4)检验葡萄糖常用新制Cu(OH)2悬浊液,将二者混合共热,观察到现象生成砖红色沉淀(或红色沉淀).
(5)乙烯通入溴的四氯化碳溶液中,反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.乙烯在一定条件下发生加聚反应生成聚乙烯,聚乙烯的结构简式为
 .
.(6)下列有关苯的叙述正确的是AB(填序号).
A.苯分子中的碳碳键是一种介于碳碳单键和碳碳双键之间的独特的键
B.苯分子里的6个碳原子和6个氢原子在同一个平面上
C.苯滴入溴水中,振荡后水层接近无色,是因为发生了加成反应.
 ;
;

 .
. ②④ C.⑤②③①④ D.④②①③⑤
②④ C.⑤②③①④ D.④②①③⑤ 论
论