题目内容
9.在SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑的反应中,氧化剂和还原剂的物质的量比为( )| A. | 24:30 | B. | 60:24 | C. | 2:1 | D. | 1:2 |
分析 反应SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑中,Si元素化合价降低,C元素化合价升高,以此解答该题.
解答 解:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑中,Si元素化合价降低,SiO2是氧化剂,C元素化合价升高,C是还原剂,由方程式可知2molC参加反应,1molSiO2被还原,则在反应中氧化剂和还原剂的物质的量之比为1:2,故D正确;
故选D.
点评 本题考查氧化还原反应,侧重于学生的分析能力和基本概念的理解和应用的考查,为高频考点,难度不大,注意从元素化合价的角度认识和解答该类题目.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列叙述中,不能说明醋酸是弱电解质的是( )
| A. | CH3COONa溶液显碱性 | |
| B. | CH3COOH能与氨水发生中和反应 | |
| C. | 室温下,0.1mol/L的CH3COOH溶液的PH为3 | |
| D. | 相同条件下,等浓度的醋酸溶液的导电能力比盐酸弱 |
17.三盐(3PbO•PbSO4•H2O)可用作聚氯乙烯的热稳定剂,200℃以上开始失去结晶水,不溶于水及有机溶剂.以200.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如图所示.
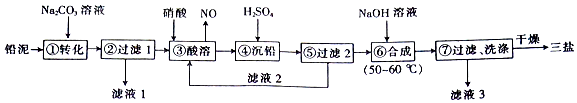
已知:PbSO4和PbCO3的溶解度和溶度积Ksp如表.
(1)步骤①转化的目的是将PbSO4转化为PbCO3,滤液1中的溶质为Na2CO3和Na2SO4(填化学式).
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是适当升温(或适当增大硝酸浓度或减小沉淀粒径等)(任写一条).其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为3Pb+8H++2NO3-=3Pb2++2NO↑+4H2O.
(3)滤液2中可循环利用的溶质的化学式为HNO3.若步骤④沉铅后的滤液中c(Pb2+)=1.82×10-5mol/L,则此时c(SO42-)=1.00×10-3mol/L.
(4)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是取少量最后一次的洗涤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全.
(5)步骤⑥合成三盐的化学方程式为4PbSO4+6NaOH$\frac{\underline{\;50~60℃\;}}{\;}$3PbO•PbSO4•H2O+3Na2SO4+2H2O,若得到纯净干燥的三盐99.Ot,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为51.75%.

已知:PbSO4和PbCO3的溶解度和溶度积Ksp如表.
| 化合物 | PbSO4 | PbCO3 |
| 溶解度/g | 1.03×10-4 | 1.81×10-7 |
| Ksp | 1.82×10-8 | 1.46×10-13 |
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是适当升温(或适当增大硝酸浓度或减小沉淀粒径等)(任写一条).其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为3Pb+8H++2NO3-=3Pb2++2NO↑+4H2O.
(3)滤液2中可循环利用的溶质的化学式为HNO3.若步骤④沉铅后的滤液中c(Pb2+)=1.82×10-5mol/L,则此时c(SO42-)=1.00×10-3mol/L.
(4)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是取少量最后一次的洗涤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全.
(5)步骤⑥合成三盐的化学方程式为4PbSO4+6NaOH$\frac{\underline{\;50~60℃\;}}{\;}$3PbO•PbSO4•H2O+3Na2SO4+2H2O,若得到纯净干燥的三盐99.Ot,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为51.75%.
14.下列说法错误的是( )
| A. | 红陶中体现红色的成分是氧化铁,氧化铁属于碱性氧化物 | |
| B. | 丝绸的主要成分是蛋白质,蛋白质是天然高分子化合物 | |
| C. | 黑火药爆炸时,碳、硫两元素被氧化 | |
| D. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了氧化还原反应 |
1.230Th和232Th是钍的两种同位素,232Th可以转化成233U.下列有关Th的说法正确的是( )
| A. | 230Th和232Th的化学性质相同 | B. | Th元素的相对原子质量是231 | ||
| C. | 232Th转化成233U是化学变化 | D. | Th元素的质量数是232 |
9.下列关于化学键的叙述正确的是( )
| A. | 全部由非金属元素组成的化合物中可含离子键 | |
| B. | H2O中所有原子都满足八电子稳定状态 | |
| C. | 两种元素构成的化合物可以含有非极性共价键 | |
| D. | CH4中所有的电子都参与形成共价键 |
10.化学与日常生活密切相关,下列有关物质应用的说法正确的是( )
| A. | 玻璃容器可长期盛放各种酸 | B. | 金刚砂主要成分为碳化硅,硬度大 | ||
| C. | 浓硫酸可刻蚀石英制艺术品 | D. | 84消毒液的有效成分是NaClO |
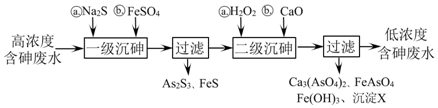
 ;②步骤2的离子方程式为12Ag++2H3As+3H2O═12Ag↓+As2O3+12H+;
;②步骤2的离子方程式为12Ag++2H3As+3H2O═12Ag↓+As2O3+12H+;