题目内容
配平化学方程式: BrF3+ H2O═ Br2+ HBrO3+ O2↑+ HF.
考点:氧化还原反应方程式的配平
专题:氧化还原反应专题
分析:该反应中Br元素化合价由+3价变为0价和+5价,部分O元素化合价由-2价变为0价,根据转移电子守恒配平方程式,据此分析解答.
解答:
解:该反应中Br元素化合价由+3价变为0价和+5价,部分O元素化合价由-2价变为0价,生成1mol溴时+3价Br得到6mol电子,生成1molHBrO3时+3价Br失去2mol电子,根据转移电子守恒知能生成1mol氧气,再结合原子守恒配平方程式为3BrF3+5H2O=HBrO3+Br2+O2↑+9HF,
故答案为:3;5;1;1;1;9.
故答案为:3;5;1;1;1;9.
点评:本题考查氧化还原反应配平,明确氧化还原反应中转移电子相等是解本题关键,注意该反应中Br元素化合价变化,题目难度不大.

练习册系列答案
相关题目
常温下,0.1mol/LHA溶液的pH>1,0.1mol/LBaOH溶液中c(OH-):c(H+)=1012,将这两种溶液等体积混合,以下离子浓度关系判断正确的是( )
| A、c(H+)<c(OH-)<c(A-)<c(B+) |
| B、c(OH-)<c(H+)<c(B+)<c(A-) |
| C、c(A-)=c(B+)>c(H+)=c(OH-) |
| D、c(A-)=c(B+)<c(H+)=c(OH-) |
下列溶液加热蒸干后,能析出溶质固体的是( )
| A、AlCl3 |
| B、K2SO3 |
| C、Fe2(SO4)3 |
| D、NH4HCO3 |
加入下列物质,能使水的电离平衡向正方向移动的是( )
| A、浓氨水 |
| B、浓盐酸 |
| C、NH4Cl固体 |
| D、NaCl固体 |
每做一次焰色反应实验,都要用一种试剂洗净铂丝,这种试剂是( )
| A、Na2CO3溶液 |
| B、NaOH溶液 |
| C、硫酸 |
| D、盐酸 |
下列物质放置在空气中,因发生氧化还原反应而变质的是( )
| A、NaCl |
| B、NaOH |
| C、Na2CO3?10H2O |
| D、Na2O2 |
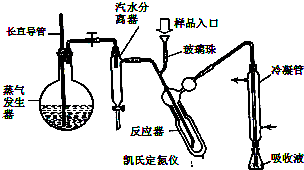 蛋白质是有机态氮的表现形式之一,蛋白质样品(或其他含氮杂质)与硫酸和催化剂一同加热消化,使含氮物质分解,分解成的氨与硫酸结合生成硫酸铵,然后碱化蒸馏使氨游离,用硼酸吸收后再用盐酸标准溶液滴定,根据酸的消耗量求得氮的质量分数,乘以换算系数(奶粉中为6.25),即得蛋白质含量.
蛋白质是有机态氮的表现形式之一,蛋白质样品(或其他含氮杂质)与硫酸和催化剂一同加热消化,使含氮物质分解,分解成的氨与硫酸结合生成硫酸铵,然后碱化蒸馏使氨游离,用硼酸吸收后再用盐酸标准溶液滴定,根据酸的消耗量求得氮的质量分数,乘以换算系数(奶粉中为6.25),即得蛋白质含量. ) B.样品入口未用蒸馏水冲洗
) B.样品入口未用蒸馏水冲洗