题目内容
下列有关的计算分析不正确的是( )
A..在反应3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O中,当有1 mol铜被氧化时,被还原的硝酸为 mol
mol
B.某溶液100 mL,其中含硫酸0.03 mol,硝酸0.04 mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015 mol
C.室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧。则a、b的关系为 a=4b+3c
D.物质的量之比为2∶5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比为1∶4
B
【解析】
试题分析:A.在反应3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O中,当有3 mol铜被氧化时,被还原的硝酸为2mol,所以若有1mol的Cu被氧化,被还原的硝酸就为 mol,正确;B. 某溶液100 mL,其中含硫酸0.03 mol,硝酸0.04 mol,若在该溶液中投入1.92 g铜粉微热,n(Cu)=0.03mol,n(H+)=0.03×2+0.04=0.1mol;n(NO3-)=0.03mol。根据反应的两种方程式可知:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知Cu不足量,产生的气体应该按照Cu来计算,n(NO)=0.02mol,错误;C. 室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧。则剩余气体是NO,根据反应方程式:3NO2+ H2O == 2HNO3+ NO可知若有c mL,相当于有NO23cmL,则变为硝酸的NO2的体积是(a-3c)ml,则消耗的氧气的体积可根据方程式4NO2+ O2+ 2H2O == 4HNO3得知:V(O2)=1/4V(NO2)= (a-3c)ml÷4=b, a-3c=4b,所以 a=4b+3c,正确;D. 物质的量之比为2∶5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则反应方程式是:4Zn+10HNO3(稀)=4Zn(NO3)2+N2O↑+5H2O.该反应中被还原的硝酸与未被还原的硝酸的物质的量之比为1∶4 ,正确。
mol,正确;B. 某溶液100 mL,其中含硫酸0.03 mol,硝酸0.04 mol,若在该溶液中投入1.92 g铜粉微热,n(Cu)=0.03mol,n(H+)=0.03×2+0.04=0.1mol;n(NO3-)=0.03mol。根据反应的两种方程式可知:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知Cu不足量,产生的气体应该按照Cu来计算,n(NO)=0.02mol,错误;C. 室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧。则剩余气体是NO,根据反应方程式:3NO2+ H2O == 2HNO3+ NO可知若有c mL,相当于有NO23cmL,则变为硝酸的NO2的体积是(a-3c)ml,则消耗的氧气的体积可根据方程式4NO2+ O2+ 2H2O == 4HNO3得知:V(O2)=1/4V(NO2)= (a-3c)ml÷4=b, a-3c=4b,所以 a=4b+3c,正确;D. 物质的量之比为2∶5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则反应方程式是:4Zn+10HNO3(稀)=4Zn(NO3)2+N2O↑+5H2O.该反应中被还原的硝酸与未被还原的硝酸的物质的量之比为1∶4 ,正确。
考点:考查有关氧化还原反应方程式的计算的知识。

 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大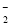 +3H2O+CO2===2Al(OH)3↓+CO
+3H2O+CO2===2Al(OH)3↓+CO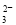
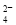 完全沉淀:Al3++Ba2++SO
完全沉淀:Al3++Ba2++SO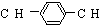 ,则M的结构式共有
,则M的结构式共有