题目内容
下列说法正确的是
A.冰熔化时,分子中H—O键发生断裂
B.HI比HF易分解,是因为HI分子间不存在氢键
C.CO2与SiO2都属于分子晶体
D.熔沸点由高到低的顺序是:金刚石>NaCl>Na
D
【解析】
试题分析:A、冰熔化时,破坏的是H2O分子间作用力,错误;B、HI比HF易分解,是因为HI分子内H—I键不牢固,错误;C、CO2为分子晶体,SiO2为原子晶体,错误;D、金刚石为原子晶体,NaCl为离子晶体,Na为金属晶体,熔断较低,则熔沸点由高到低的顺序是:金刚石>NaCl>Na,正确。
考点:本题考查物质结构与性质。

练习册系列答案
相关题目
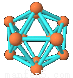
观察下列模型并结合有关信息,判断有关说法正确的是
| 硼晶体的结构单元 | SF6分子 | S8分子 | NaCl |
结构模型示意图 |
|
|
|
|
备注 | 熔点1873K | / | 易溶于CS2 | / |
A.单质硼属分子晶体,其结构单元B12中含有30个B-B键,含20个正三角形
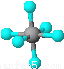
B.SF6是由极性键构成的分子
C.固态硫S8属于原子晶体
D.NaCl熔化和溶于水均能产生自由移动的离子,且破坏的是同种作用力,NaCl晶胞中每个Na+周围最近且等距离的Na+有6个
t℃时,10mL0.4mol?L?1H2O2溶液发生催化分【解析】
2H2O2=2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表
t/min | 0 | 2 | 4 | 6 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~2min H2O2平及反应速率比4~6min快
B.0~6min的平均反应速率V(H2O2)≈3.3×10-2mol?L-1?min-1
C.反应至6min时,C(H2O2)=0.3mol?L?1
D.反应至6min时,H2O2分解了50%


 CO2(g) + H2(g) △H<0,下列措施能提高反应速率的有 (不定项选择)。
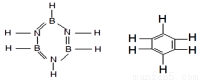
CO2(g) + H2(g) △H<0,下列措施能提高反应速率的有 (不定项选择)。 等相继被发现。下列有关说法中,正确的是
等相继被发现。下列有关说法中,正确的是