题目内容
下列反应的离子方程式正确的是( )
| A、向浓度均为0.1 mol?L-1的KNO3和KHSO4的混合溶液中加入铜片:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| B、向Na2CO3浴液中逐滴加入少量稀盐酸:CO32-+2H+═H2O+CO2↑ |
| C、二氧化硫通人氯化铁溶液中:2Fe3++SO2+2H2O═2Fe2++4H++SO42- |
| D、在FeI2溶液中滴少量溴水:2Fe2++Br2═2Fe3++2Br- |
考点:离子方程式的书写
专题:
分析:A.反应生成NO;
B.少量盐酸,生成氯化钠和碳酸氢钠;
C.发生氧化还原反应,生成硫酸亚铁;
D.少量溴水只氧化碘离子.
B.少量盐酸,生成氯化钠和碳酸氢钠;
C.发生氧化还原反应,生成硫酸亚铁;
D.少量溴水只氧化碘离子.
解答:
解:A.浓度均为0.1mol?L-1的KNO3和KHSO4的混合溶液相当于稀硝酸的溶液,与铜发生的反应应为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故A错误;
B.向Na2CO3溶液中逐滴加入少量稀盐酸不会生成二氧化碳,应为CO32-+H+=HCO3-,故B错误;
C.二氧化硫通人氯化铁溶液中的离子反应为2Fe3++SO2+2H2O═2Fe2++4H++SO42-,故C正确;
D.I-的还原性强于Fe2+,在FeI2溶液中滴入少量溴水时,先被氧化的应为I-,故正确离子反应为Br2+2I-=2Br-+I2,故D错误;
故选C.
B.向Na2CO3溶液中逐滴加入少量稀盐酸不会生成二氧化碳,应为CO32-+H+=HCO3-,故B错误;
C.二氧化硫通人氯化铁溶液中的离子反应为2Fe3++SO2+2H2O═2Fe2++4H++SO42-,故C正确;
D.I-的还原性强于Fe2+,在FeI2溶液中滴入少量溴水时,先被氧化的应为I-,故正确离子反应为Br2+2I-=2Br-+I2,故D错误;
故选C.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
下列实验合理的是( )
A、 量取500ml盐酸 |
B、 检验Fe2+ |
C、 制乙酸乙酯 |
D、 分离汽油和水 |
化学与生活息息相关,以下日常生活的做法或判断合理的是( )
| A、新铝锅使用后颜色变暗用砂纸打磨 |
| B、某矿泉水暴露于空气中变黄是因为水中可能含有Fe2+ |
| C、氯气泄漏后应逆风向低处跑 |
| D、用米汤检验某食盐是否为加碘盐 |
化学概念在逻辑上存在如图所示的三种关系,下列说法错误的是( )
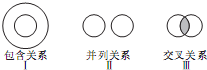

| A、烃与烷烃属于I |
| B、电解质与非电解质属于Ⅱ |
| C、离子反应与氧化还原反应属于Ⅲ |
| D、酸性氧化物与非金属氧化物属于I |
下列指定反应的离子方程式正确的是( )
| A、用白醋除铁锈:Fe2O3?xH2O+6H+=(3+x)H2O+2Fe3+ |
| B、用强碱溶液吸收工业制取硝酸尾气:NO+NO2+2OH-=2NO3-+H2O |
| C、将少量SO2气体通入氨水中:SO2+NH3?H2O=NH4++HSO3- |
| D、向稀硫酸中加入少量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
 固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )| A、有O2放电的a极为电池的负极 |
| B、O2-移向电池的正极 |
| C、b极对应的电极反应为2H2-4e-+2O2-═2H2O |
| D、a极对应的电极反应为O2+2H2O+4e-═4OH- |
含NO3-的工业废水会造成水体富营养化,可利用如下反应将其转化为无毒、无污染的N2:A1+口+口→口十口+口,反应中涉及到的另外3种微粒是H2O、A1(OH)3、OH-.下列说法正确的是( )
| A、反应中的Al被还原,NO3-是还原剂 |
| B、三种反应物分别是Al、NO3-和OH- |
| C、若有1 mol Al参加反应,则有0.6 mol NO3-被还原 |
| D、随着反应的进行,溶液的碱性逐渐减弱 |
NA为阿伏伽德罗常数,下列说法正确的是( )
| A、同温同压同体积的CO2和SO2所含氧原子数均为2NA |
| B、32gCu与S完全反应转移的电子数为NA(相对原子质量 Cu:64) |
| C、1L 1.0mol?L-1NH4Cl与2L 0.5mol?L-1NH4Cl溶液含NH4+数目相同 |
| D、25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.1NA |