题目内容
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“=”).
(2)前2s内的平均反应速率υ(N2)= .
(3)在该温度下,反应的平衡常数K= .
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 .
A.选用更有效的催化剂B.升高反应体系的温度
C.降低反应体系的温度D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
①请在上表空格中填入剩余的实验条件数据.
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号.

| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol/L) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)(mol/L) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)在上述条件下反应能够自发进行,则反应的△H
(2)前2s内的平均反应速率υ(N2)=
(3)在该温度下,反应的平衡常数K=
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
A.选用更有效的催化剂B.升高反应体系的温度
C.降低反应体系的温度D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
| 实验 编号 |
T(℃) | NO初始浓度 (mol/L) |
CO初始浓度 (mol/L) |
催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号.

考点:化学平衡的计算,化学平衡的影响因素,物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)发生反应2NO+2CO?2CO2+N2,该反应为气体减少,△S<0非自发,由△G=△H-T△S可知,该反应一定为放热才有可能自发;
(2)根据v=
计算v(NO),再利用速率之比等于化学计量数之比计算v(N2);
(3)由表中数据可知,4s时反应到达平衡状态,平衡时c(NO)=1.00×10-4mol/L,故△c(NO)=1.00×10-3mol/L-1.00×10-4mol/L=9×10-4mol/L,利用三段式计算出平衡时各组分的平衡浓度,代入平衡常数表达式计算;
(4)达到平衡时提高NO转化率,应使平衡向正反应移动,根据平衡移动原理结合选项解答,注意不能只增大NO的浓度;
(5)①目的是研究温度和催化剂的比表面积对反应速率的影响,所以在实验时应保持NO、CO的初始浓度不变,让温度、比表面积其中一个量变化,Ⅰ、Ⅱ研究的是催化剂的比表面积对速率的影响,因此可确定Ⅱ中温度为280℃;
②Ⅰ、Ⅱ研究的是催化剂的比表面积对速率的影响,因此可确定Ⅱ中温度为280℃,
Ⅱ、Ⅲ的催化剂比表面积相同,研究的是温度对速率的影响,
Ⅰ、Ⅲ催化剂的比表面积不同,温度不同,研究温度、催化剂的比表面积对反应速率的影响,
绘图时,要注意达平衡的时间、平衡浓度的相对大小:
Ⅱ与Ⅰ温度相同,平衡不移动,平衡浓度相同,但Ⅱ催化剂比表面积增大,达平衡时间短;
Ⅲ与Ⅱ的催化剂比表面积相同,Ⅲ温度高,温度升高,不仅达平衡时间缩短,平衡向左移动,使NO的平衡浓度也增大.
(2)根据v=
| △c |
| △t |
(3)由表中数据可知,4s时反应到达平衡状态,平衡时c(NO)=1.00×10-4mol/L,故△c(NO)=1.00×10-3mol/L-1.00×10-4mol/L=9×10-4mol/L,利用三段式计算出平衡时各组分的平衡浓度,代入平衡常数表达式计算;
(4)达到平衡时提高NO转化率,应使平衡向正反应移动,根据平衡移动原理结合选项解答,注意不能只增大NO的浓度;
(5)①目的是研究温度和催化剂的比表面积对反应速率的影响,所以在实验时应保持NO、CO的初始浓度不变,让温度、比表面积其中一个量变化,Ⅰ、Ⅱ研究的是催化剂的比表面积对速率的影响,因此可确定Ⅱ中温度为280℃;
②Ⅰ、Ⅱ研究的是催化剂的比表面积对速率的影响,因此可确定Ⅱ中温度为280℃,
Ⅱ、Ⅲ的催化剂比表面积相同,研究的是温度对速率的影响,
Ⅰ、Ⅲ催化剂的比表面积不同,温度不同,研究温度、催化剂的比表面积对反应速率的影响,
绘图时,要注意达平衡的时间、平衡浓度的相对大小:
Ⅱ与Ⅰ温度相同,平衡不移动,平衡浓度相同,但Ⅱ催化剂比表面积增大,达平衡时间短;
Ⅲ与Ⅱ的催化剂比表面积相同,Ⅲ温度高,温度升高,不仅达平衡时间缩短,平衡向左移动,使NO的平衡浓度也增大.
解答:
解:(1)发生反应2NO+2CO?2CO2+N2,该反应为气体减少,△S<0非自发,由△G=△H-T△S可知,该反应一定为放热才有可能自发,即△H<0,
故答案为:<;
(2)v(NO)=
=3.75×10-4mol/(L?s),速率之比等于化学计量数之比,所以v(N2)=
v(NO)=
×3.75×10-4mol/(L?s)=1.875×10-4mol/(L?s),
故答案为:1.875×10-4mol/(L?s);
(3)由表中数据可知,4s时反应到达平衡状态,平衡时c(NO)=1.00×10-4mol/L,故△c(NO)=1.00×10-3mol/L-1.00×10-4mol/L=9×10-4mol/L,则:
2NO+2CO?2CO2+N2,
开始(×10-4mol/L):10 36 0 0
变化(×10-4mol/L):9 9 9 4.5
平衡(×10-4mol/L):1 27 9 4.5
所以该温度下平衡常数k=
=5000
故答案为:5000;
(4)A、催化剂不影响平衡的移动,故A错误,
B、该反应放热,升高温度平衡向逆反应移动,NO的转化率降低,故B错误,
C、该反应放热,降温平衡正向移动,NO转化率增大,故C正确,
D、缩小体积,增大压强,平衡向体积减小的方向运动,即正向移动,NO转化率增大,故D正确,
故答案为:CD;
(5)①目的是研究温度和催化剂的比表面积对反应速率的影响,所以在实验时应保持NO、CO的初始浓度不变,让温度、比表面积其中一个量变化,Ⅰ、Ⅱ研究的是催化剂的比表面积对速率的影响,因此可确定Ⅱ中温度为280℃,
故答案为:Ⅱ、280;1.20×10-3;5.80×10-3;
Ⅲ、1.20×10-3;5.80×10-3;
②Ⅰ、Ⅱ研究的是催化剂的比表面积对速率的影响,
Ⅱ、Ⅲ的催化剂比表面积相同,研究的是温度对速率的影响,
Ⅰ、Ⅲ催化剂的比表面积不同,温度不同,研究温度、催化剂的比表面积对反应速率的影响,
绘图时,要注意达平衡的时间、平衡浓度的相对大小:
Ⅱ与Ⅰ温度相同,平衡不移动,平衡浓度相同,但Ⅱ催化剂比表面积增大,达平衡时间短,
Ⅲ与Ⅱ的催化剂比表面积相同,Ⅲ温度高,温度升高,不仅达平衡时间缩短,平衡向左移动,使NO的平衡浓度也增大,
三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图为:
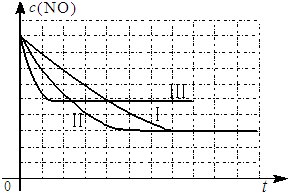
故答案为: .
.
故答案为:<;
(2)v(NO)=
| 1×10-3mol/L-2.5×10-4mol/L |
| 2s |
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:1.875×10-4mol/(L?s);
(3)由表中数据可知,4s时反应到达平衡状态,平衡时c(NO)=1.00×10-4mol/L,故△c(NO)=1.00×10-3mol/L-1.00×10-4mol/L=9×10-4mol/L,则:
2NO+2CO?2CO2+N2,
开始(×10-4mol/L):10 36 0 0
变化(×10-4mol/L):9 9 9 4.5
平衡(×10-4mol/L):1 27 9 4.5
所以该温度下平衡常数k=
| (9×10-4)2×4.5×10-4 |
| (1×10-4)2×(27×10-4)2 |
故答案为:5000;
(4)A、催化剂不影响平衡的移动,故A错误,
B、该反应放热,升高温度平衡向逆反应移动,NO的转化率降低,故B错误,
C、该反应放热,降温平衡正向移动,NO转化率增大,故C正确,
D、缩小体积,增大压强,平衡向体积减小的方向运动,即正向移动,NO转化率增大,故D正确,
故答案为:CD;
(5)①目的是研究温度和催化剂的比表面积对反应速率的影响,所以在实验时应保持NO、CO的初始浓度不变,让温度、比表面积其中一个量变化,Ⅰ、Ⅱ研究的是催化剂的比表面积对速率的影响,因此可确定Ⅱ中温度为280℃,
故答案为:Ⅱ、280;1.20×10-3;5.80×10-3;
Ⅲ、1.20×10-3;5.80×10-3;
②Ⅰ、Ⅱ研究的是催化剂的比表面积对速率的影响,
Ⅱ、Ⅲ的催化剂比表面积相同,研究的是温度对速率的影响,
Ⅰ、Ⅲ催化剂的比表面积不同,温度不同,研究温度、催化剂的比表面积对反应速率的影响,
绘图时,要注意达平衡的时间、平衡浓度的相对大小:
Ⅱ与Ⅰ温度相同,平衡不移动,平衡浓度相同,但Ⅱ催化剂比表面积增大,达平衡时间短,
Ⅲ与Ⅱ的催化剂比表面积相同,Ⅲ温度高,温度升高,不仅达平衡时间缩短,平衡向左移动,使NO的平衡浓度也增大,
三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图为:

故答案为:
 .
.
点评:本题考查化学平衡的计算、平衡移动影响因素、影响速率因素探究实验,题目计算量大、阅读量大,是对学生心理素质的考验,难度较大,注意三段式解题法的理解运用,全面掌握基础知识.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
下列有关化学用语正确的是( )
| A、核内有8个中子的碳原子:8C |
| B、CS2的结构式:S-C-S |
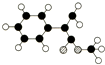
C、乙烯的比例模型: |
D、NH4Br的电子式: |
下列物质的分类组合全部正确的是( )
| 编组 | 强电解质 | 弱电解质 | 非电解质 |
| A | NaCl | HF | Cl2 |
| B | H2SO4 | BaCO3 | CO2 |
| C | AgCl | HClO | Cu |
| D | Ba(OH)2 | H2S | 蔗糖 |
| A、A | B、B | C、C | D、D |
下列离子方程式与所述事实相符且正确的是( )
A、用二氧化硫水溶液吸收溴蒸气:SO2+Br2+2H2O=
| ||||||
| B、在碳酸氢钠溶液中加入过量的氢氧化钡溶液:Ba2++OH-+HCO3-=BaCO3↓+H2O | ||||||
C、用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NO3)2++2OH-
| ||||||
D、等物质的量浓度、等体积FeCl3、NaBr、CuSO4的混合溶液电解,最初发生的反应为::Cu2++2CI-
|
下列过程中,没有明显实验现象的是( )
| A、向Fe(NO3)2溶液中滴加稀硫酸 |
| B、将盐酸滴入NaAlO2溶液中 |
| C、向碳酸氢钠溶液中滴加氢氧化钠溶液 |
| D、加热溶有SO2的品红溶液 |
下列物质的水溶液呈现酸性的是( )
| A、小苏打 | B、生石灰 |
| C、食醋 | D、烧碱 |
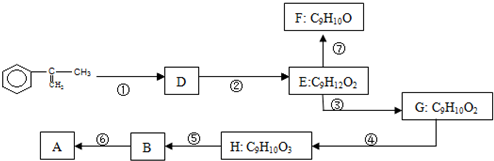
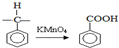
 化学-选修有机化学基础
化学-选修有机化学基础 拟从
拟从 出发合成A.
出发合成A.