题目内容
13.写出下列反应的离子方程式(1)硫酸氢钠与氢氧化钠的反应OH-+H+═H2O
(2)碳酸氢钠与盐酸的反应HCO3-+H+═H2O+CO2↑
(3)盐酸与碳酸钙的反应CaCO3+2H+═H2O+CO2↑+Ca2+
(4)铁与稀硫酸的反应Fe+2H+═Fe2++H2↑
(5)硫酸与氢氧化铜的反应Cu(OH)2+2H+═Cu2++2H2O.
分析 (1)硫酸氢钠与氢氧化钠反应生成硫酸钠和水;
(2)碳酸氢钠与盐酸反应生成氯化钠、二氧化碳气体和水;
(3)碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水,碳酸钙需要保留化学式;
(4)铁与稀硫酸反应生成硫酸亚铁和氢气;
(5)氢氧化铜为难溶物,离子方程式中需要保留化学式.
解答 解:(1)硫酸氢钠与氢氧化钠的反应的离子方程式为:OH-+H+═H2O,
故答案为:OH-+H+═H2O;
(2)碳酸氢钠与盐酸反应的实质为碳酸氢根离子与氢离子反应生成二氧化碳和水,反应的离子方程式为:HCO3-+H+═H2O+CO2↑,
故答案为:HCO3-+H+═H2O+CO2↑;
(3)碳酸钙为难溶物,需要保留化学式,二者反应的离子方程式为:CaCO3+2H+═H2O+CO2↑+Ca2+,
故答案为:CaCO3+2H+═H2O+CO2↑+Ca2+;
(4)铁与稀硫酸反应的离子方程式为:Fe+2H+═Fe2++H2↑,
故答案为:Fe+2H+═Fe2++H2↑;
(5)硫酸与氢氧化铜反应生成硫酸铜和水,反应的离子方程式为:Cu(OH)2+2H+═Cu2++2H2O,
故答案为:Cu(OH)2+2H+═Cu2++2H2O.
点评 本题考查了离子方程式的书写,题目难度中等,明确离子方程式的书写原则为解答关键,注意掌握发生反应的实质,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
8.已知稀硝酸和稀硫酸组成的混酸中c(NO3-)+c(SO42-)=5mol•L-1,若取一定量的混酸溶解铜粉达到最大值(假设还原产物只有NO),则混酸中HNO3、H2SO4的物质的量浓度之比为( )
| A. | 1:1 | B. | 3:2 | C. | 2:3 | D. | 2:1 |
5.下列说法正确的是( )
| A. | 18g水含有的原子数为NA | |
| B. | 4g金属钙变成钙离子时失去的电子数为0.1NA | |
| C. | 1molO2的质量等于1mol氧原子的质量 | |
| D. | 24gO2和24gO3所含的原子数目相等 |
5.甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.该反应的离子方程式为2MnO4-+5H2C2O4+6H+═2Mn2++10CO2+8H2O
设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小
某同学进行实验,实验装置如图1.其中A、B的成分见表
(1)该实验的目的是探究草酸浓度和催化剂对化学反应速率的影响.
(2)实验开始前需要检查气密性.分液漏斗中A溶液应该一次性加入(填“一次性”或“逐滴滴加”)
(3)完成该实验还需要秒表(填仪器名称),实验结束后读数前需要移动量气管,使两个量气管的液面相平.
(4)请在图2中,画出实验②、③中CO2体积随时间变化的预期结果示意图.
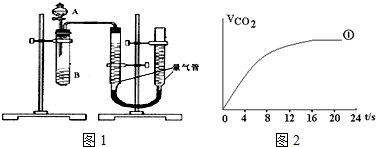
乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率为了探究KMnO4与H2C2O4浓度对反应速率的影响,某同学在室温下完成以下实验
(5)X=5,4号实验中始终没有观察到溶液褪色,你认为可能的原因是KMnO4过量.
(6)2号反应中,H2C2O4的反应速率为0.00625mol/(L•s).
(7)在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,
溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
结合实验目的与表中数据,你得出的结论是温度不是反应速率突然加快的原因.
(8)从影响化学反应速率的因素看,你的猜想还可能是反应产物的影响.
设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小
某同学进行实验,实验装置如图1.其中A、B的成分见表
| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液 |
| ② | 2mL 0.1mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液 |
| ③ | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液和少量MnSO4 |
(2)实验开始前需要检查气密性.分液漏斗中A溶液应该一次性加入(填“一次性”或“逐滴滴加”)
(3)完成该实验还需要秒表(填仪器名称),实验结束后读数前需要移动量气管,使两个量气管的液面相平.
(4)请在图2中,画出实验②、③中CO2体积随时间变化的预期结果示意图.

乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率为了探究KMnO4与H2C2O4浓度对反应速率的影响,某同学在室温下完成以下实验
| 实验编号 | 1 | 2 | 3 | 4 |
| 水/mL | 10 | 5 | 0 | X |
| 0.5mol/L H2C2O4/mL | 5 | 10 | 10 | 5 |
| 0.2mol/L KMnO4/mL | 5 | 5 | 10 | 10 |
| 时间/s | 40 | 20 | 10 | --- |
(6)2号反应中,H2C2O4的反应速率为0.00625mol/(L•s).
(7)在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,
溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
| 时间/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26.5 | 27 | 27 |
(8)从影响化学反应速率的因素看,你的猜想还可能是反应产物的影响.