题目内容
13.某烃结构式如下: -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )| A. | 所有碳原子不可能在同一平面上 | B. | 所有碳原子可能在同一条直线上 | ||
| C. | 碳原子同一平面上至少有9个 | D. | 所有原子可能在同一平面上 |
分析 根据共面结构的基本物质:乙烯、乙炔、苯环等的结构来回答,乙烯为平面形,苯为平面形,乙炔为直线形,也在同一平面上.
解答 解:A.有机物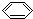 -C≡C-CH=CH-CH3中,具有苯环、乙烯的共面结构以及乙炔的共线结构,所以苯环的6个碳原子一定共面,具有乙烯结构的后4个碳原子一定共面,具有乙炔结构的两个碳原子(倒数第四个和倒数第五个)一定共线,所有的碳原子可以共面,故A错误;
-C≡C-CH=CH-CH3中,具有苯环、乙烯的共面结构以及乙炔的共线结构,所以苯环的6个碳原子一定共面,具有乙烯结构的后4个碳原子一定共面,具有乙炔结构的两个碳原子(倒数第四个和倒数第五个)一定共线,所有的碳原子可以共面,故A错误;
B.炔烃中两个碳乙基炔烃相连的乙烯基中1个碳可以共平面,另外乙基与此取代基处于对位上,故与乙基相连的苯环上的C和乙基山1个碳也与其共直线,故总共可以有6个碳原子共直线,故B错误;
C.苯为平面结构,乙炔为直线型分子,取代乙炔分子中氢原子的位置在同一直线上,碳原子同一平面上至少有9个,故C正确;
D.甲烷是正四面体结构,与碳原子相连的四个原子不可能在同一平面上,故D错误.
故选C.
点评 本题主要考查有机物的基本结构知识,难度不大,注意甲烷是正四面体结构,与碳原子相连的四个原子不可能在同一平面上.

练习册系列答案
相关题目
3.用硫酸酸化的草酸(H2C2O4,二元弱酸)溶液能将KMnO4溶液中的MnO4-转化为Mn2+.某化学小组研究发现,少量MnSO4可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,完成以下实验设计表.
表中a、b的值分别为:a=50、b=10
(2)该反应的离子方程式5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O.
(3)若t1<t2,则根据实验①和②得到的结论是溶液的pH对该反应的速率有影响.
(4)请你设计实验验证MnSO4对该反应起催化作用,完成下表中内容.
(5)化学小组用滴定法测定KMnO4溶液物质的量浓度:取ag草酸晶体(H2C2O4•2H2O,摩尔质量126g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定两次,平均消耗KMnO4溶液VmL.滴定到达终点的现象是:加入最后一滴KMnO4溶液,溶液呈浅红色,且30秒内不褪色;
实验中所需的定量仪器有托盘天平、250mL容量瓶、(酸式)滴定管(填仪器名称).
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,完成以下实验设计表.
| 实验 编号 | 温度 | 初始pH | 0.1mol/L草酸溶液/mL | 0.01mol/L KMnO4溶液 体积/mL | 蒸馏水 体积/mL | 待测数据(反应混合液褪色 时间/s) |
| ① | 常温 | 1 | 20 | 50 | 30 | t1 |
| ② | 常温 | 2 | 20 | 50 | 30 | t2 |
| ③ | 常温 | 2 | 40 | a | b | t3 |
(2)该反应的离子方程式5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O.
(3)若t1<t2,则根据实验①和②得到的结论是溶液的pH对该反应的速率有影响.
(4)请你设计实验验证MnSO4对该反应起催化作用,完成下表中内容.
| 实验方案(不要求写出具体操作过程) | 预期实验结果和结论 |
往反应混合液中加入少量MnSO4固体,控制其他反应条件与实验①相同, 进行对比实验 | 若反应混合液褪色时间小于实验①中的t1,则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
实验中所需的定量仪器有托盘天平、250mL容量瓶、(酸式)滴定管(填仪器名称).
4.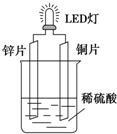 以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.某实验兴趣小组做完实验后,在读书卡片上记录如下:
以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.某实验兴趣小组做完实验后,在读书卡片上记录如下:
(1)在卡片上,记录合理的是⑤⑥(填序号).
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是锌片不纯(在锌片表面形成原电池).
(3)其他条件相同情况下,产生气泡的速率比单一锌片快(填“快”或“慢”),
如果将锌片换成铁片,电路中的电流方向不变(填“变”或“不变”).
(4)如果把硫酸换成硫酸铜溶液,猜测铜片(填“锌片”或“铜片”)变厚,原因是Cu2++2e-=Cu(用电极方程式表示).实验结束后称得两极质量差12.9g,假设初始时Zn片与Cu片质量相等,则反应中转移的电子的物质的量为0.2mol.
(5)有同学利用原电池原理,将A、B、C、D四种金属设计下表中装置进行实验用以判断四种金属的活泼性强弱.
根据以上现象,判断四种金属活泼性由强到弱的顺序是D>A>B>C.
 以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.某实验兴趣小组做完实验后,在读书卡片上记录如下:
以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.某实验兴趣小组做完实验后,在读书卡片上记录如下:| 实验后的记录: ①Zn片发生还原反应,Cu片发生氧化反应 ②H+向负极移动 ③LED发光时,电子流动方向Zn→导线→Cu,再经溶液流回铜片 ④溶液的pH变小 ⑤若有1mol电子流过导线,则产生H2为0.5mol. ⑥装置中存在“化学能→电能→光能”的转换 |
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是锌片不纯(在锌片表面形成原电池).
(3)其他条件相同情况下,产生气泡的速率比单一锌片快(填“快”或“慢”),
如果将锌片换成铁片,电路中的电流方向不变(填“变”或“不变”).
(4)如果把硫酸换成硫酸铜溶液,猜测铜片(填“锌片”或“铜片”)变厚,原因是Cu2++2e-=Cu(用电极方程式表示).实验结束后称得两极质量差12.9g,假设初始时Zn片与Cu片质量相等,则反应中转移的电子的物质的量为0.2mol.
(5)有同学利用原电池原理,将A、B、C、D四种金属设计下表中装置进行实验用以判断四种金属的活泼性强弱.
| 序号 | 甲 | 乙 | 丙 |
| 装置 | 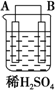 | 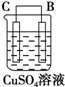 | 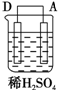 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
8.下列有机物的命名正确的是( )
| A. | 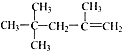 2,2,4-三甲基一4 一戊烯 2,2,4-三甲基一4 一戊烯 | |
| B. |  l,3,4一三甲苯 l,3,4一三甲苯 | |
| C. | CH3CH(CH3)CH(OH)CH3 2-甲基-3-丁醇 | |
| D. |  3,3,4-三甲基己烷 3,3,4-三甲基己烷 |
18.有反应mA(g)+nB(g)?wC(g),测得在同一时间内A每分钟减少0.15mol•L-1,B每分钟减少0.05mol•L-1,C每分钟增加0.1mol•L-1,则下列叙述不正确的是( )
| A. | m:n:w=3:1:2 | |
| B. | 体积和温度不变时,若在前10s内A减少了x mol,则B在前20s内减少$\frac{2x}{3}$ mol | |
| C. | 体积和温度不变时,随反应进行压强逐渐下降,一段时间后压强保持恒定不变 | |
| D. | 单位时间内反应物浓度的减少大于生成物浓度的增加 |
5.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染.下列做法不符合绿色化学理念的是( )
| A. | 研制水溶剂涂料替代有机溶剂涂料 | |
| B. | 用可降解塑料生产包装盒或快餐盒 | |
| C. | 用反应:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O 制备硫酸铜 | |
| D. | 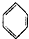 +CH2=CH2→ +CH2=CH2→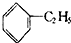 |
3.现有Na2CO3、H2SO4、Ba(OH)2三种溶液,它们的体积与物质的量浓度都相等.以不同顺序将它们中的两种混合,若产生沉淀则过滤,再将滤液与第三种溶液混合,那么最终所得的溶液( )
| A. | 可能呈酸性 | B. | 不可能呈碱性 | ||
| C. | 可能呈中性或碱性 | D. | 不可能呈中性 |