题目内容
某元素位于第三周期第ⅣA族.下列叙述不正确的是( )
| A、该元素是金属元素 |
| B、该元素原子的核电荷数为14 |
| C、该元素原子核外有3个电子层 |
| D、该元素原子不容易得到或者失去最外层电子 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:元素位于第三周期第ⅣA族,为Si元素,质子数为14,以此来解答.
解答:
解:A,为Si元素,属于非金属元素,故A错误;
B.Si的质子数为14,则该元素原子的核电荷数为14,故B正确;
C.位于第三周期,原子结构中有3个电子层,故C正确;
D.最外层有4个电子,则不容易得到或者失去最外层电子,故D正确;
故选A.
B.Si的质子数为14,则该元素原子的核电荷数为14,故B正确;
C.位于第三周期,原子结构中有3个电子层,故C正确;
D.最外层有4个电子,则不容易得到或者失去最外层电子,故D正确;
故选A.
点评:本题考查元素的位置和原子结构,为高频考点,把握周期数、族序数与原子结构中的电子层、最外层电子数的关系为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
水壶长时间使用后,会形成一层水垢(主要成分为CaCO3).厨房中的下列物质可用来清除水垢的是( )
| A、白醋 | B、食盐 | C、料酒 | D、小苏打 |
下列说法正确的( )
| A、50 mL 18.4 mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46 NA |
| B、常温下浓硫酸能使铝发生钝化,可在常温下用铝制贮罐贮运浓硫酸 |
| C、浓硫酸能使蔗糖炭化体现了它的吸水性 |
| D、浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2 |
下列离子方程式正确的是( )
| A、氨水溶液中通人足量二氧化硫气体:OH-+SO2=HSO3-- | ||||
B、用惰性电极电解饱和氯化钠溶液:2Cl-+2H +
| ||||
| C、用稀硝酸洗涤试管内壁的银镜:3Ag+4H++NO3-=3Ag++NO↑+2H2O | ||||
| D、次氯酸钙溶液中通人少量二氧化硫:Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO |
0.1mol NaHCO3中含有( )
| A、0.1 mol Na+ |
| B、0.05 mol CO32- |
| C、6.02×1023个 O |
| D、0.2 mol H |
某短周期元素原子的最外电子层只有2个电子,该元素不可能是( )
| A、0族元素 |
| B、ⅡA族元素 |
| C、第二周期元素 |
| D、ⅣA族元素 |
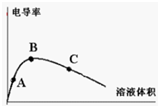 某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.