题目内容
12.短周期元素甲和乙,甲原子的最外层电子数为a,次外层电子数为b;乙原子的M层电子数为(a-b),L层电子数为(a+b).则甲、乙两元素形成的化合物具有的性质是( )| A. | 与水反应 | B. | 与氢氧化钠溶液反应 | ||
| C. | 与硫酸反应 | D. | 与前三种物质均能反应 |
分析 短周期元素甲和乙,甲原子的最外层电子数为a,次外层电子数为b;乙原子的M层电子数为(a-b),L层电子数为(a+b),则a+b=8,所以甲原子有2个电子层,故b=2,所以a=6,故甲为氧元素;乙原子的M层电子数为(a-b)=6-2=4,则乙为 硅元素.则甲、乙两元素形成的化合物为二氧化硅.结合物质的性质判断.
解答 解:A.甲乙两元素形成的化合物是二氧化硅,难溶于水,且不与水反应,故A错误;
B.二氧化硅能与氢氧化钠反应生成硅酸钠,故B正确;
C.二氧化硅不与硫酸反应,只与HF反应,故C错误;
D.由以上分析可知,故D错误,
故选B.
点评 本题考查核外电子排布规律、元素化合物的性质,难度不大,理解核外电子排布规律、元素推断是关键.

练习册系列答案
相关题目
17.在有机化工中,氯气是合成塑料、橡胶、农药和染料等的重要原料.下列关于氯气性质的描述不正确的是( )
| A. | 无气味 | B. | 能溶于水 | C. | 能与水反应 | D. | 能与铜反应 |
4.某粒子的结构示意图为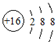 ,关于该粒子的说法正确的是( )
,关于该粒子的说法正确的是( )
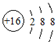 ,关于该粒子的说法正确的是( )
,关于该粒子的说法正确的是( )| A. | 核电荷数为18 | B. | 核外有3个电子层 | ||
| C. | 属于非金属元素的原子 | D. | 在化学反应中易得2个电子 |
2.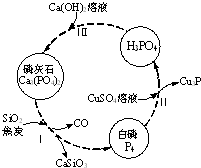 磷及部分重要化合物的相互转化如图所示.
磷及部分重要化合物的相互转化如图所示.
(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为0.05mol.
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有Ca (H2PO4)2、CaHPO4.
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
(3)磷灰石中,碳元素的质量分数为1.66%%(保留两位小数).
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4114.87g(保留两位小数).
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值.
 磷及部分重要化合物的相互转化如图所示.
磷及部分重要化合物的相互转化如图所示.(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为0.05mol.
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有Ca (H2PO4)2、CaHPO4.
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
| 成分 | CaO | P2O5 | SO3 | CO2 |
| 质量分数(%) | 47.30 | 28.40 | 3.50 | 6.10 |
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4114.87g(保留两位小数).
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值.