��Ŀ����
9����A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������A��һ��ͬλ��ԭ�������ӣ�A��Eͬ���壬BԪ���γɵĻ�����������ࣻCԪ�ص�����������Ӧˮ�������⻯���ܷ�Ӧ�����Σ�DԪ��ԭ�ӵ������������Ӳ�����3�������û�ѧ����ش��������⣺��1��CԪ�������ڱ��е�λ�õڶ����ڵ�VA���壮
��2���Ƚ�D��E����Ԫ�����Ӱ뾶�Ĵ�С����������ӷ��ţ�O2-��Na+��
��3��Ԫ��A��C���γ�ԭ�Ӹ�����Ϊ2��1�ķ��ӣ��÷��ӵĵ���ʽΪ
 ��
����֪0.4molҺ̬������������Һ̬A2D2��Ӧ��������̬C2����̬A2D���ų�256.6KJ����������д���÷�Ӧ���Ȼ�ѧ����ʽN2H4��l��+2H2O2��l���TN2��g��+4H2O��g������H=-641.5KJ��mol-1��
��4��CԪ�ص�����������Ӧˮ���������⻯�����ɵ��Σ���ˮ��Һ�����ԣ�ѡ����ԡ��������ԡ������ԡ����������ӷ���ʽ����ԭ��NH4++H2O?NH3•H2O+H+
��5�����п�����֤C��D��Ԫ��ԭ������ǿ������ʵ��BC����д��ţ�
A���Ƚ�������Ԫ�ص���̬�⻯���÷е�
B���Ƚ�ֻ��������Ԫ�����γɵĻ������еĻ��ϼ�
C���Ƚ�������Ԫ�صļ���̬�⻯����ȶ���
D���Ƚ�������Ԫ�ص�����������Ӧˮ���������
��6��A��B��C��D����Ԫ����ɵ�һ�ֻ�����F�������ԭ����֮��Ϊ5��1��1��3��F��Һ������EDA��ϡ��Һ��ϣ������ӷ���ʽΪNH4++HCO3-+2OH-=CO32-+NH3•H2O+H2O����
��7������Ԫ���γɵĵ��ʻ��������ͼת����ϵ��
��$\stackrel{O_{2}}{��}$��$\stackrel{O_{2}}{��}$��$\stackrel{H_{2}O}{��}$��
������Ϊǿ�ᣬ������NO
������Ϊǿ�д������ˮ��Ӧ�����ӷ���ʽ2Na2O2+2H2O=4Na++4OH-+O2����
���� ��A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������A��һ��ͬλ��ԭ�������ӣ�AΪHԪ�أ�BԪ���γɵĻ�����������࣬BΪCԪ�أ�CԪ�ص�����������Ӧˮ�������⻯���ܷ�Ӧ�����Σ�CΪNԪ�أ�DԪ��ԭ�ӵ������������Ӳ�����3����DΪO��A��Eͬ���壬EΪ��Ԫ�أ�
��� �⣺��A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������A��һ��ͬλ��ԭ�������ӣ�AΪHԪ�أ�BԪ���γɵĻ�����������࣬BΪCԪ�أ�CԪ�ص�����������Ӧˮ�������⻯���ܷ�Ӧ�����Σ�CΪNԪ�أ�DԪ��ԭ�ӵ������������Ӳ�����3����DΪO��A��Eͬ���壬EΪ��Ԫ�أ�
��1��CԪ�ص�����������Ӧˮ�������⻯���ܷ�Ӧ�����Σ�CΪNԪ�أ�NԪ�������ڱ��еĵڶ����ڵ�VA���壻
�ʴ�Ϊ���ڶ����ڵ�VA���壻
��2���������������Ӿ�����ͬ��������Ų���������11�����ӣ�������8�����ӣ��������Ӱ뾶��O2-��Na+��
�ʴ�Ϊ��O2-��Na+��
��3��Ԫ��A��C���γ�ԭ�Ӹ�����Ϊ2��1�ķ��ӣ�ΪN2H4���ǵ�ԭ�Ӻ͵�ԭ���γ�һ�����ۼ���ʣ��ۼ�����ԭ���γɹ��ۼ�������ʽΪ
�ʴ�Ϊ��
��4��CԪ�ص�����������Ӧˮ���������⻯�����ɵ���Ϊ����泥������Ϊǿ�������Σ�ˮ�������ԣ����ӷ���ʽ��NH4++H2O?NH3•H2O+H+��
�ʴ�Ϊ��NH4++H2O?NH3•H2O+H+��
��5��A��Ԫ�طǽ�����ǿ������̬�⻯��ķе��أ���A��ѡ��
B��̼�����γɹ��ۻ�������Ը��ۣ�˵�����õ��Ӷ�ƫ��������ԭ�ӵõ�������ǿ����Bѡ��
C����̬�⻯��Խ�ȶ���Ԫ�طǽ�����Խǿ����Cѡ��
D��������ۺ����ᣬ��D��ѡ��
��ѡ��BC��
��6��a��b��c��dԪ�طֱ�Ϊ��H��C��N��O��ԭ�Ӹ�����Ϊ5��1��1��3�Ļ�����ΪNH4HCO3��
NH4HCO3���������Ʒ�Ӧ����̼���ư�����ˮ����Ӧ�����ӷ���ʽΪ��NH4++HCO3-+2OH-=CO32-+NH3•H2O+H2O��
�ʴ�Ϊ��NH4++HCO3-+2OH-=CO32-+NH3•H2O+H2O��
��7���ٵ�����������Ӧ����һ��������һ��������������Ӧ���ɶ�������������������ˮ��Ӧ�������ᣬ��������Ϊǿ�ᣬ������NO��
�ʴ�Ϊ��NO��
���������������·�Ӧ���������ƣ��������������������ɹ������ƣ�����������ˮ��Ӧ�����������ƺ����������ӷ���ʽ��2Na2O2+2H2O=4Na++4OH-+O2����
�ʴ�Ϊ��2Na2O2+2H2O=4Na++4OH-+O2����
���� ���⿼��λ�ýṹ���ʵ�Ӧ�ã��漰���û�ѧ���Ԫ�ػ��������ʡ����ӷ���ʽ����д�ȣ���ȷԪ�ص�λ���ƶϳ���Ԫ���ǽ��Ĺؼ�����ϤԪ�ص����ʼ�����������ʼ��ɽ����Ŀ�Ѷ��еȣ�

| ʵ����� | �� | �� | �� |
| �Ͻ�����/mg | 255 | 385 | 459 |
| �����������/mL | 280 | 336 | 336 |
��1��Ҫ�����������ʵ���Ũ�ȣ�������Ϊ�������ݵ��������һ������õ���������ʵ���Ũ��Ϊ1.5mol/L��
��2����Ͻ���Mg��Al�����ʵ���֮�ȣ����п���Ϊ�������ݵ������Ǽף���õ�Mg��Al���ʵ���֮��Ϊ1��1��
| A�� | ��100 mL | B�� | ����100 mL | C�� | ����100 mL | D�� | ����100/�� mL |
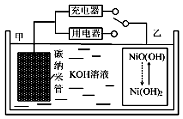 2016��8�£����Ϲ������ƻ������й��������⾭��ʾ�����С��ڽ�������仧����������H2��̼���ܵȲ��������Ķ��ε�ص�ԭ����ͼ��ʾ������˵����ȷ���ǣ�������
2016��8�£����Ϲ������ƻ������й��������⾭��ʾ�����С��ڽ�������仧����������H2��̼���ܵȲ��������Ķ��ε�ص�ԭ����ͼ��ʾ������˵����ȷ���ǣ�������| A�� | �ŵ�ʱ���缫��ӦΪ��NiO��OH��+H2O+e?�TNi��OH��2+OH? | |
| B�� | �ŵ�ʱ���缫Ϊ������OH?�����ҵ缫 | |
| C�� | ����ܷ�ӦΪH2+2NiO��OH��$?_{�ŵ�}^{���}$ 2Ni��OH��2 | |
| D�� | ���ʱ����ص�̼�缫��ֱ����Դ���������� |
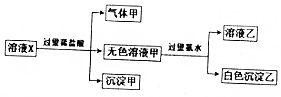 ˮ��Һ��ֻ������K+��Mg2+��AlO2-��Al3+��SiO32-��CO32-��SO42-�е����������ӣ�ijͬѧ����Һ����������ʵ�飺�����жϴ�����ǣ�������
ˮ��Һ��ֻ������K+��Mg2+��AlO2-��Al3+��SiO32-��CO32-��SO42-�е����������ӣ�ijͬѧ����Һ����������ʵ�飺�����жϴ�����ǣ�������| A�� | ��ҺX���ܺ���Mg2+��Al3+ | |
| B�� | ������ֻ�����ǹ������ | |
| C�� | ����������ɣ�������ҺX��һ������CO32- | |
| D�� | ����ȷ��SO42-�Ƿ��������ҺX�� |
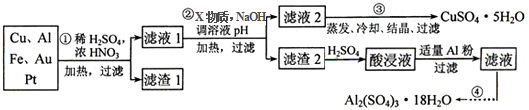
��Ҫ��ش��������⣺
��1������1�д��ڵĽ�����Au��Pt��
��2����֪�������pH���±���
| �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.7 |
| Cu2+ | 4.9 | 6.7 |
| Al3+ | 3.0 | 4.4 |
a�����Ը��������Һ b��Ư�� c������ d��˫��ˮ
��������Ӧ������ҺpH�ķ�Χ��4.4��pH��4.9��
��3��������Һ2�мȲ�����Fe2+�ֲ�����Fe3+�IJ��������Ǣ�ȡ������Һ���Թ��У��������м�������KSCN��Һ�������Һ�����֤��������Fe3+���ۼ�������Һ�е������Ƶ���ˮ�������Һ�����֤��������Fe2+��
��4����һ�����ӷ���ʽ��ʾ�����Һ�м����������۵ķ�Ӧ��Al+Fe3+=Fe+Al3+��
��5����CuSO4•5H2O�Ʊ�CuSO4ʱ��Ӧ��CuSO4•5H2O�������������������ƣ��м�����ˮ��
��6������ijЩ������ʹ�õĸ��������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ���ܳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ 3Zn+2K2FeO4+8H2O$?_{���}^{�ŵ�}$3Zn��OH��2+2Fe��OH��3+4KOH���õ�طŵ�ʱ������ӦʽΪZn-2e-+2OH-=Zn��OH��2��ÿ��1mol K2FeO4����ԭ��ת�Ƶ��ӵ����ʵ���Ϊ3mol�����ʱ������ӦʽΪFe��OH��3+5OH--3e-=FeO42-+4H2O��