题目内容
完成下列填空:
(1)电离方程式:NaHCO3NH3?H2O NaHSO4
(2)选择适宜的物质完成下列反应,并写出有关反应的化学方程式
Cu+2Ag+=Cu 2++2Ag
CO32-+2H+=CO2+H2O
(3)完成下列离子反应方程式
OH-+ =CO32-+ (系数不改变)
CaCO3+ =CO2↑+ + .
(1)电离方程式:NaHCO3NH3?H2O
(2)选择适宜的物质完成下列反应,并写出有关反应的化学方程式
Cu+2Ag+=Cu 2++2Ag
CO32-+2H+=CO2+H2O
(3)完成下列离子反应方程式
OH-+
CaCO3+
考点:离子方程式的书写,电离方程式的书写
专题:离子反应专题,电离平衡与溶液的pH专题
分析:(1)强电解质完全电离,用“═”,弱电解质不完全电离,用“?”,遵循电荷守恒、原子守恒,注意原子团不可拆分;
(2)Cu与硝酸银的离子反应为Cu+2Ag+=Cu2++2Ag,碳酸钠与盐酸反应的离子反应为CO32-+2H+=CO2+H2O;
(3)氢氧根离子与碳酸氢根离子反应生成碳酸根离子和水;碳酸钙和盐酸反应生成氯化钙、水、二氧化碳.
(2)Cu与硝酸银的离子反应为Cu+2Ag+=Cu2++2Ag,碳酸钠与盐酸反应的离子反应为CO32-+2H+=CO2+H2O;
(3)氢氧根离子与碳酸氢根离子反应生成碳酸根离子和水;碳酸钙和盐酸反应生成氯化钙、水、二氧化碳.
解答:
解:(1)NaHCO3为强电解质,电离方程式为NaHCO3═Na++HCO3-,
NH3?H2O为弱电解质,电离方程式为NH3?H2O?NH4++OH-,
NaHSO4为强电解质,电离方程式为NaHSO4═Na++H++SO42-,
故答案为:NaHCO3═Na++HCO3-;NH3?H2O?NH4++OH-;NaHSO4═Na++H++SO42-;
(2)Cu+2Ag+=Cu 2++2Ag的化学反应如Cu+2AgNO3=2Ag+Cu(NO3)2,
CO32-+2H+=CO2+H2O的化学反应如Na2CO3+2HCl=2NaCl+H2O+CO2↑,
故答案为:Cu+2AgNO3=2Ag+Cu(NO3)2;Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)氢氧根离子与碳酸氢根离子反应生成碳酸根离子和水,离子反应为OH-+HCO3-=CO32-+H2O;碳酸钙和盐酸反应生成氯化钙、水、二氧化碳,离子反应为CaCO3+2H+=CO2+H2O+Ca2+,故答案为:HCO3-;H2O;2H+;H2O;Ca2+.
NH3?H2O为弱电解质,电离方程式为NH3?H2O?NH4++OH-,
NaHSO4为强电解质,电离方程式为NaHSO4═Na++H++SO42-,
故答案为:NaHCO3═Na++HCO3-;NH3?H2O?NH4++OH-;NaHSO4═Na++H++SO42-;
(2)Cu+2Ag+=Cu 2++2Ag的化学反应如Cu+2AgNO3=2Ag+Cu(NO3)2,
CO32-+2H+=CO2+H2O的化学反应如Na2CO3+2HCl=2NaCl+H2O+CO2↑,
故答案为:Cu+2AgNO3=2Ag+Cu(NO3)2;Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)氢氧根离子与碳酸氢根离子反应生成碳酸根离子和水,离子反应为OH-+HCO3-=CO32-+H2O;碳酸钙和盐酸反应生成氯化钙、水、二氧化碳,离子反应为CaCO3+2H+=CO2+H2O+Ca2+,故答案为:HCO3-;H2O;2H+;H2O;Ca2+.
点评:本题考查化学用语,为高频考点,侧重电离方程式、离子方程式、化学反应方程式书写的考查,注意(2)中由离子反应书写化学反应的答案不唯一,有利于学生基础知识的夯实,题目难度不大.

练习册系列答案
相关题目
下列溶液中,阴离子浓度最大的是( )
| A、0.5mol/L HCl溶液50mL |
| B、0.6mol/L Al2(SO4)3溶液40mL |
| C、0.7mol/L NaCl溶液70mL |
| D、0.8mol/L Na2CO3溶液60mL |
将过量Cl2通入NaBr和NaI的混合液中,然后把混合溶液蒸干,再将剩余残渣灼烧,最后留下的物质( )
| A、NaBr,NaI |
| B、NaCl,NaBr |
| C、NaCl |
| D、NaCl,I2 |
工业上利用硅的氧化物制取硅单质,主要反应为:SiO2+2C
Si+2CO↑.该反应中,还原剂是 (填化学式),被还原的物质是 (填化学式);若反应中消耗了1mol C,则生成 mol Si.
| ||
有下列4种燃料电池的工作原理示意图,其中正极反应的产物为水的是( )
A、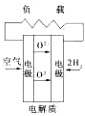 固化氧化物燃料电池 |
B、 碱性氢氧化物电池 |
C、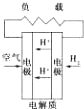 质子交换膜燃料电池 |
D、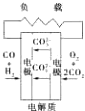 熔融盐燃料电池 |
 某离子反应中涉及N2、H2O、ClO-、H+、NH4+、Cl-六种微粒.其中N2的物质的量随时间变化的曲线如图.
某离子反应中涉及N2、H2O、ClO-、H+、NH4+、Cl-六种微粒.其中N2的物质的量随时间变化的曲线如图.