题目内容
某实验小组设计用50mL 1.0mol?L-1盐酸跟50mL 1.1mol?L-1氢氧化钠溶液在如图所示装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题: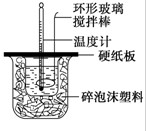
(1)写出仪器环形玻璃搅拌棒的作用
(2)碎泡沫塑料(或纸条)及泡沫塑料板的作是 .
(3)本实验中用稍过量的NaOH的原因教材中说是为保证盐酸完全被中和.试问:盐酸在反应中若因为有放热现象,而造成少量盐酸在反应中挥发,则测得的中和热 (填“偏大”、“偏小”或“不变”).
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热 (填“偏大”、“偏小”或“不变”).

(1)写出仪器环形玻璃搅拌棒的作用
(2)碎泡沫塑料(或纸条)及泡沫塑料板的作是
(3)本实验中用稍过量的NaOH的原因教材中说是为保证盐酸完全被中和.试问:盐酸在反应中若因为有放热现象,而造成少量盐酸在反应中挥发,则测得的中和热
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热
考点:中和热的测定
专题:实验题
分析:(1)根据中和热的测定原理分析解答;
(2)中和热测定实验成败的关键是保温工作;
(3)根据少量盐酸在反应中挥发,反应的盐酸偏少,放出的热量偏小;
(4)没有用水洗涤温度计上的盐酸溶液,导致盐酸的物质的量偏小,放出的热量偏小.
(2)中和热测定实验成败的关键是保温工作;
(3)根据少量盐酸在反应中挥发,反应的盐酸偏少,放出的热量偏小;
(4)没有用水洗涤温度计上的盐酸溶液,导致盐酸的物质的量偏小,放出的热量偏小.
解答:
解:(1)中和热的测定须测量酸碱反应的热效应,使用环形玻璃搅拌棒能使溶液上下混合均匀,保证溶液上下的温度达到一致,减少实验误差,
故答案为:使溶液上下混合均匀,保证溶液上下的温度达到一致;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,故答案为:减少热量的损失;
(3)少量盐酸在反应中挥发,盐酸挥发吸收热量,且盐酸偏少,放出的热量偏小,测得的中和热数值偏低,故答案为:偏小;
(4)没有用水洗涤温度计上的盐酸溶液,导致盐酸的物质的量偏小,放出的热量偏小,测得的中和热数值偏小,故答案为:偏小.
故答案为:使溶液上下混合均匀,保证溶液上下的温度达到一致;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,故答案为:减少热量的损失;
(3)少量盐酸在反应中挥发,盐酸挥发吸收热量,且盐酸偏少,放出的热量偏小,测得的中和热数值偏低,故答案为:偏小;
(4)没有用水洗涤温度计上的盐酸溶液,导致盐酸的物质的量偏小,放出的热量偏小,测得的中和热数值偏小,故答案为:偏小.
点评:本题考查中和热的测定,题目难度大,注意理解中和热测定原理以及测定反应热的误差等问题.

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )

| A、该硫酸的物质的量浓度为9.2mol/L |
| B、1molZn与足量的该硫酸反应产生2g氢气 |
| C、配制200mL4.6mol/L的稀硫酸需取该硫酸500mL |
| D、该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2mol/L |
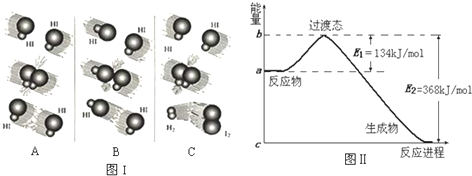
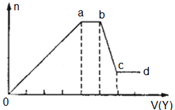 某无色稀溶液X中,可能含有下表所列离子中的某几种.
某无色稀溶液X中,可能含有下表所列离子中的某几种. X、Y、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+的3d轨道中有9个电子.
X、Y、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+的3d轨道中有9个电子.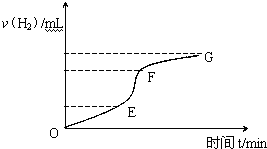 用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
用纯净的锌粒与稀盐酸反应制取氢气气体,请回答: