题目内容
14.将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是( )| A. | 消耗的氧化剂n(HNO3):两者相同 | |
| B. | 消耗硝酸的物质的量:前者多,后者少 | |
| C. | 反应生成气体的颜色:前者浅,后者深 | |
| D. | 反应中转移的电子总数:前者多,后者少 |
分析 浓硝酸氧化性强于稀硝酸,所以铜与浓硝酸反应更剧烈,相同质量的铜分别和过量的浓硝酸、稀硝酸反应,Cu完全反应,转移电子数相同,生成硝酸铜相同,由3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O、Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O可知消耗浓硝酸多,以此来解答.
解答 解:A.由3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O、Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O可知,设Cu均为3mol时,前者氧化剂为2mol,后者氧化剂为6mol,故A错误;
B.由3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O、Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O可知,设Cu为3mol,前者消耗硝酸为8mol,后者消耗硝酸为12mol,故B正确;
C.铜与浓硝酸反应生成红棕色二氧化氮,与稀硝酸反应生成无色一氧化氮,故C错误;
D.相同质量的铜分别和过量的浓硝酸、稀硝酸反应,Cu完全反应,转移电子数相同,故D错误;
故选B.
点评 本题考查Cu与浓硝酸、稀硝酸的反应,为高频考点,把握发生的反应、物质的量关系为解答的关键,侧重分析与计算能力的考查,注意物质的量关系,题目难度不大.

练习册系列答案
相关题目
20.合成抗哮喘及抗过敏药普仑司特的某种中间体结构如图:

有关该中间体的说法正确的是( )

有关该中间体的说法正确的是( )
| A. | 该分子中含有1个手性碳原子 | |
| B. | 能发生氧化、取代、加成反应 | |
| C. | 1mol该化合物与足量NaOH溶液反应,最多消耗4molNaOH | |
| D. | 1mol该化合物与足量浓溴水反应,最多消耗1molBr2 |
5.对于aA(g)+bB(g)?cC(g)反应,改变某一变量(条件)得到如图象(p 表示压强,T 表示温度,n 表示物质的量,á 表示平衡转化率).根据图象,下列判断正确的是( )


| A. | 反应 I:若 p1>p2,则 a+b>c | |
| B. | 反应Ⅱ:此反应的△H>0,且 T1<T2 | |
| C. | 反应Ⅲ:表示t1 时刻一定是使用催化剂对反应速率的影响 | |
| D. | 反应Ⅳ:表示t1时刻增大 B 的浓度对反应速率的影响 |
2.下列微粒中与NH4+具有相同质子数和电子数的是( )
| A. | H3O+ | B. | H2O | C. | Ne | D. | OH- |
9.下列关于铵盐的叙述:
①铵盐中氮元素化合价都是-3价;
②铵盐都是晶体,都易溶于水;
③铵盐与碱共热放出氨气;
④铵盐都不能与酸反应;
⑤铵盐都易分解.
其中正确的是( )
①铵盐中氮元素化合价都是-3价;
②铵盐都是晶体,都易溶于水;
③铵盐与碱共热放出氨气;
④铵盐都不能与酸反应;
⑤铵盐都易分解.
其中正确的是( )
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ②③⑤ |
19.在光照条件下,将1mol CH4与1mol Cl2混合充分反应后,得到的混合物是( )
| A. | CH3Cl HCl | |
| B. | CH3Cl CH2Cl2 CHCl3CCl4 HCl | |
| C. | CH3Cl CH2Cl | |
| D. | CH3Cl CH2Cl2 CHCl3 CCl4 CH4HCl |
6.下列有关叙述不正确的是( )
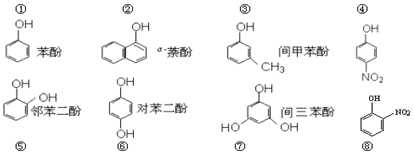
⑨HNO3 ⑩NH3.

⑨HNO3 ⑩NH3.
| A. | 能形成分子内氢键的有⑤⑧⑨ | |
| B. | 能形成分子间氢键有①②③④⑥⑦⑩ | |
| C. | 根据氢键形成的条件,可以推测还有元素Li的原子可以代替氢原子而形成类似氢键的结构 | |
| D. | C2H6O分子中同时存在极性键、非极性键和氢键 |
3.下列叙述正确的是( )
| A. | 渗析实验可以鉴别胶体和溶液 | |
| B. | 由分子组成的物质中一定存在共价键 | |
| C. | 水的电离是吸热过程,升高温度,水的离子积增大、pH减小 | |
| D. | 用金属活动性顺序可解释反应:Na(l)+KCl(l)═NaCl(l)+K(g) |
 ①根据图所示,写出反应的热化学方程式:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41 kJ/mol.
①根据图所示,写出反应的热化学方程式:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41 kJ/mol.