题目内容
7.下列说法正确的是( )| A. | 水库中的钢闸门通常连接锌块,是采用了牺牲阳极的阴极保护法 | |
| B. | 化学电源都是一次能源 | |
| C. | 铁的表面镀铜的过程中,铜极连接电源负极 | |
| D. | 合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其组成成分金属强 |
分析 A.水库中的钢闸门通常连接锌块,锌为负极,保护铁不受腐蚀;
B.一次能源是指直接从自然界获得的能源;
C.电镀时,镀层作阳极,镀件作阴极;
D.合金熔点低,耐腐蚀性强.
解答 解:A.水库中的钢闸门通常连接锌块,锌为负极,保护铁不受腐蚀,为牺牲阳极的阴极保护法,故A正确;
B.一次能源是指直接从自然界获得的能源,而化学电源是将化学能转化为电能,所以都不是一次能源,故B错误;
C.电镀时,镀层作阳极,镀件作阴极,所以铁表面镀铜时,铜作阳极,连接电源正极,故C错误;
D.合金熔点低,耐腐蚀性强,则合金的熔点都低于它的成分金属,故D错误;
故选:A.
点评 本题考查了金属的腐蚀与防护、一次能源的判断、合金的性质以及电镀原理等,明确原电池和电解池原理是解本题关键,难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
18.原子序数依次增大的A、B、C、D、E五种短周期元素.A、B可形成密度为0.76g/L(标准状况下) 的气体,C的最外层电子数为其内层电子数的3倍,A与D、C与E同主族.下列说法正确的是( )
| A. | D2E2和A2C2两种化合物对应晶体中的化学键类型相同 | |
| B. | 只含A、B、C三种元素的某化合物水溶液,可能呈碱性或酸性 | |
| C. | 原子半径大小:D>B>C;简单离子半径大小:D+>E2->C2- | |
| D. | A2C的稳定性强于A2E、沸点高于A2E,均因为A-C键键能大于A-E键键能 |
2.下列溶液中c(Cl-) 与50mL 1mol/L 氯化铝溶液中的c(Cl-) 相等的是( )
| A. | 150 mL 1mol/L氯化钠溶液 | B. | 75 mL 2mol/L氯化铵溶液 | ||
| C. | 150 mL 1mol/L氯化铁溶液 | D. | 75 mL 1mol/L氯化亚铁溶液 |
12.决定气体体积大小的主要因素是( )
①气体分子的数目
②气体分子的直径
③气体分子间的距离
④气体分子的质量.
①气体分子的数目
②气体分子的直径
③气体分子间的距离
④气体分子的质量.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.8 g铁粉与50 mL 4 mol•L-1盐酸反应转移电子的数目为0.15NA | |
| B. | 常温下1 L pH=13的氢氧化钠溶液中由水电离出的H+的数目为0.1NA | |
| C. | 标准状况下,8.96 L氢气、一氧化碳的混合气体完全燃烧,消耗氧分子的数目为0.2NA | |
| D. | 1.2 g金刚石与石墨混合物中含有碳碳单键的数目为0.4NA |
16.下列说法正确的是( )
| A. | 氧化铜的摩尔质量是80 g | B. | 氨气的摩尔质量是17 mol | ||
| C. | 氧气的摩尔质量是32 g•mol-1 | D. | 1 mol氢原子的质量是2 g |
17.利用如图所示装置进行下列实验,根据现象能得出相应实验结论的是( )
| ①中的反应物 | ②中的现象 | 实验结论 | 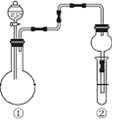 | |
| A | 纯碱、稀硫酸 | 硅酸钠溶液中出现白色沉淀 | 酸性:硫酸>碳酸>硅酸 | |
| B | MnO2、浓盐酸 | 淀粉KI溶液变蓝 | Cl2有氧化性 | |
| C | Na2SO3、硫酸 | 溴水褪色 | SO2有漂白性 | |
| D | Cu、硝酸 | 红棕色气体 | ①中硝酸为浓硝酸 |
| A. | A | B. | B | C. | C | D. | D |
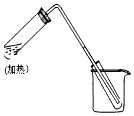 如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题:
如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题: