题目内容
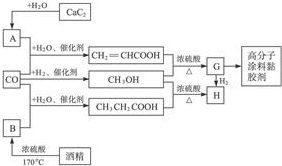
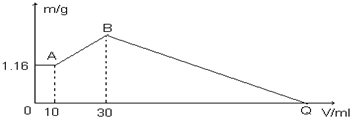
20.把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol/LHCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.试回答:(1)A点的沉淀物的化学式为Mg(OH)2.
(2)原混合物中AlCl3的质量是2.67g.
(3)Q点HCl溶液加入量是130ml.
分析 向水中固体组成的混合物溶液中加入盐酸时,0-A时没有沉淀生成,说明溶液中NaOH过量,则铝离子完全转化为偏铝酸根离子,溶液中存在的沉淀为Mg(OH)2;
A-B段,盐酸和偏铝酸钠反应生成氢氧化铝沉淀,离子反应方程式为H2O+AlO2-+H+=Al(OH)3↓,B点溶液中存在的溶质是氯化钠,沉淀为Mg(OH)2、Al(OH)3;
B-C过程中,氢氧化镁和氢氧化铝都与盐酸反应生成氯化铝和氯化镁,所以Q点溶液中的溶质是氯化铝、氯化镁和氯化钠.
解答 解:(1)向水中固体组成的混合物溶液中加入盐酸时,0-A时没有沉淀生成,说明此时盐酸和氢氧化钠反应,即:NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,溶液中NaOH过量,此时溶液中铝离子为偏铝酸根离子,溶液中存在的沉淀为Mg(OH)2;
故答案为:Mg(OH)2;
(2)A-B段有沉淀生成,应为盐酸和偏铝酸钠反应生成氢氧化铝沉淀,离子反应方程式为AlO2-+H++H2O=Al(OH)3↓,B点溶液中存在的溶质是氯化钠,沉淀为Mg(OH)2、Al(OH)3,离子反应方程式为:H2O+AlO2-+H+=Al(OH)3↓,根据HCl的体积知,n(AlO2-)=n(HCl)=1mol/L×(0.03-0.01)L=0.02mol,根据Al原子守恒得n(AlCl3)=n(AlO2-)=0.02mol,m(AlCl3)=n(AlCl3)•M=0.02mol×133.5g/mol=2.67g,
故答案为:2.67g;
(3)A点沉淀的是氢氧化镁,则n(Mg(OH)2)=$\frac{m}{M}$=$\frac{1.16g}{58g/mol}$=0.02mol,根据Mg原子守恒得n(MgCl2)=n(Mg(OH)2)=0.02mol;
B-Q过程中,氢氧化镁和氢氧化铝都与盐酸反应生成氯化铝和氯化镁,所以Q点溶液中的溶质是氯化铝、氯化镁和氯化钠,原反应物为:NaOH、MgCl2、AlCl3和盐酸,对比知反应前后MgCl2、AlCl3不变,实际上相当于氢氧化钠和盐酸的反应,所以Q点可以看做氢氧化钠和盐酸二者恰好反应,n(NaOH)=n(HCl),B点溶液中存在的溶质是氯化钠,由Na+离子和Cl-离子守恒得,原混合物中:n(NaOH)=n(NaCl)=n(Cl-)=2n(MgCl2)+3n(AlCl3)+n(HCl)=0.02mol×2+0.02mol×3+0.03L×1mol/L=0.13mol,
则V(HCl)=$\frac{0.13mol}{1mol/L}$=0.13L=130mL,
故答案为:130.
点评 本题考查混合物反应的有关计算,题目难度中等,明确曲线变化趋势及每段发生的化学反应是解本题关键,知道拐点代表的含义及溶液中溶质的成分,结合方程式、原子守恒对有关问题进行分析从而得出正确答案,注意掌握守恒思想在化学计算中的应用,试题培养了学生的化学计算能力.

 阅读快车系列答案
阅读快车系列答案| A. | 等浓度时水溶液碱性:NaHCO3>Na2CO3 | |
| B. | 热稳定性:NaHCO3>Na2CO3 | |
| C. | 与盐酸溶液反应的速率(快慢):NaHCO3<Na2CO3 | |
| D. | 等质量的Na2CO3、NaHCO3分别与足量的盐酸反应,NaHCO3产生的CO2多 |
| A. | 质子数为53、中子数为78的碘原子:${\;}_{53}^{131}$I | |
| B. | 硫离子的结构示意图: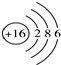 | |
| C. | H2O2的结构式:H-O-H-O | |
| D. | NH4I的电子式: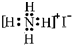 |
| A. | 用氧化铝与水反应制取氢氧化铝 | B. | 氢氧化铝用于治疗胃酸过多 | ||
| C. | 氧化铁可用作红色颜料 | D. | 铁制容器可盛装烧碱溶液 |
| A. | Fe2O3 | B. | FeO | C. | Fe(OH)3 | D. | Fe3O4 |
| A. | FeO与稀硝酸反应:FeO+2H+═Fe2++H2O | |
| B. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的稀醋酸:CO32-+H+═HCO3- | |
| D. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ |
| A. | “地沟油”禁止食用,但可以用来制皂 | |
| B. | 安全、合理的使用核能有利于降低碳排放 | |
| C. | 采用“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 | |
| D. | 吸烟不会造成室内PM 2.5污染 |
| A. | 某溶液的pH=7,则该溶液为中性溶液 | |
| B. | 一定温度下,向AgCl饱和溶液中加入少量NaCl固体,Ksp(AgCl)减小 | |
| C. | 常温下,反应X(s)+Y(l)═2Z(g)不能自发,则该反应的△H>0 | |
| D. | 常温下,0.01mol/L的NaOH溶液中由水电离的c(H+)=1.0×10-2mol/L |