题目内容
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),下列中和反应结论正确的是( )
| 选项 | 起始浓度/(mol?L-1) | 反应后溶液的pH | 结论 | |
| c(HA) | c(KOH) | |||
| A. | 0.1 | 0.1 | 7 | HA为弱酸 |
| B. | 0.1 | 0.1 | 9 | c(K+)<c(A-) |
| C. | 0.2 | 0.1 | 6 | HA为强酸 |
| D. | 0.2 | 0.1 | 8 | C(A-)<c(HA) |
| A、A | B、B | C、C | D、D |
考点:酸碱混合时的定性判断及有关ph的计算,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A、由表中组数据可知,一元酸HA和KOH溶液等体积、等浓度混合,二者恰好反应,KA溶液pH=7,说明溶液呈中性,这种盐为强碱强酸盐;
B、由表中组数据可知,一元酸HA和KOH溶液等体积、等浓度混合,二者恰好反应,KA溶液pH=9,说明溶液呈碱性,这种盐为强碱弱酸盐;
C、一元酸HA和KOH溶液等体积、HA浓度0.2mol/L,而KOH的浓度为0.1mol/L,混合,二者完全反应,得到等物质量浓度的HA和KA,以酸的电离为主,故溶液呈酸性,所以酸可以是强酸,也可以是弱酸;
D、一元酸HA和KOH溶液等体积、HA浓度0.2mol/L,而KOH的浓度为0.1mol/L,混合,二者完全反应,得到等物质量浓度的HA和KA,以酸的电离为主,故溶液呈酸性,所以C(A-)<c(HA).
B、由表中组数据可知,一元酸HA和KOH溶液等体积、等浓度混合,二者恰好反应,KA溶液pH=9,说明溶液呈碱性,这种盐为强碱弱酸盐;
C、一元酸HA和KOH溶液等体积、HA浓度0.2mol/L,而KOH的浓度为0.1mol/L,混合,二者完全反应,得到等物质量浓度的HA和KA,以酸的电离为主,故溶液呈酸性,所以酸可以是强酸,也可以是弱酸;
D、一元酸HA和KOH溶液等体积、HA浓度0.2mol/L,而KOH的浓度为0.1mol/L,混合,二者完全反应,得到等物质量浓度的HA和KA,以酸的电离为主,故溶液呈酸性,所以C(A-)<c(HA).
解答:
解:A、由表中组数据可知,一元酸HA和KOH溶液等体积、等浓度混合,二者恰好反应,KA溶液pH=7,说明溶液呈中性,这种盐为强碱强酸盐,所以HA为强酸,故A错误;
B、由表中组数据可知,一元酸HA和KOH溶液等体积、等浓度混合,二者恰好反应,KA溶液pH=9,说明溶液呈碱性,这种盐为强碱弱酸盐,酸根离子要水解,则c(K+)>c(A-),故B错误;
C、一元酸HA和KOH溶液等体积、HA浓度0.2mol/L,而KOH的浓度为0.1mol/L,混合,二者完全反应,得到等物质量浓度的HA和KA,以酸的电离为主,故溶液呈酸性,所以酸可以是强酸,也可以是弱酸,故C错误;
D、一元酸HA和KOH溶液等体积、HA浓度0.2mol/L,而KOH的浓度为0.1mol/L,混合,二者完全反应,得到等物质量浓度的HA和KA,以酸的电离为主,故溶液呈酸性,所以C(A-)<c(HA),故D正确;
故选D.
B、由表中组数据可知,一元酸HA和KOH溶液等体积、等浓度混合,二者恰好反应,KA溶液pH=9,说明溶液呈碱性,这种盐为强碱弱酸盐,酸根离子要水解,则c(K+)>c(A-),故B错误;
C、一元酸HA和KOH溶液等体积、HA浓度0.2mol/L,而KOH的浓度为0.1mol/L,混合,二者完全反应,得到等物质量浓度的HA和KA,以酸的电离为主,故溶液呈酸性,所以酸可以是强酸,也可以是弱酸,故C错误;
D、一元酸HA和KOH溶液等体积、HA浓度0.2mol/L,而KOH的浓度为0.1mol/L,混合,二者完全反应,得到等物质量浓度的HA和KA,以酸的电离为主,故溶液呈酸性,所以C(A-)<c(HA),故D正确;
故选D.
点评:本题考查离子浓度大小比较、溶液PH值、盐类水解等,难度中等,判断一元酸HA是弱酸为解题关键.

练习册系列答案
相关题目
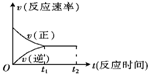 一定条件下的某可逆反应中,正、逆反应速率[用v(正)、v(逆)表示]随时间变化如图所示,则下列说法中错误的是( )
一定条件下的某可逆反应中,正、逆反应速率[用v(正)、v(逆)表示]随时间变化如图所示,则下列说法中错误的是( )| A、在O~t1间,v(正)>v(逆) |
| B、在t1~t2间,v(正)=v(逆) |
| C、在t1时刻,反应在给定的条件下达到了最大限度 |
| D、在t1以后,平衡状态不受任何因素的影响 |
 早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融)═4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH═Fe3O4+2H2↑+4Na↑.下列有关说法正确的是( )
早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融)═4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH═Fe3O4+2H2↑+4Na↑.下列有关说法正确的是( )| A、电解熔融氢氧化钠制钠,阳极发生电极反应为:4OH--4e-=O2↑+2H2O |
| B、盖?吕萨克法制钠原理是利用铁的还原性比钠强 |
| C、若戴维法与盖?吕萨克法制得等量的钠,则两反应中转移的电子总数也相同 |
| D、目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阴极,铁为阳极 |
在一定条件下的密闭容器中,加入2molSO2和1molO2,充分反应后能证明2SO2+O2?2SO3 是可逆反应的事实是( )
| A、O2仍为1mol |
| B、SO2仍为2mol |
| C、SO2完全转化为SO3 |
| D、SO2、O2和SO3同时存在 |
关于丙烯醛(CH2=CH-CHO)的叙述不正确的是( )
| A、可使溴水和KMnO4溶液褪色 |
| B、与足量的H2加成生成丙醛 |
| C、能发生银镜反应 |
| D、在一定条件下可氧化成酸 |
钴在自然界中只存在一种稳定的同位素Co-59,而Co-60是一种穿透力很强的核辐射元素,可用来治疗癌症.下列说法正确的是( )
| A、 27 59Co 原子核内含有59个质子 |
| B、Co-59和Co-60互为同位素 |
| C、 27 60Co 原子核内含有43个中子 |
| D、 27 60Co 原子的最外层电子数为27 |
下列有关实验、工业生产说法不正确的是( )
| A、海洋植物具有富集碘的能力,因此从海产品中提取碘是工业上获取碘的重要途径 |
| B、乙醚、乙醇和苯等一些有机溶剂极易被引燃,使用时必须远离明火和热源,用毕立即塞紧瓶塞 |
| C、当吸滤瓶内液面高度快达到支管口位置时,应拔掉链接支管口的橡皮管,并从支管口倒出 |
| D、用分液漏斗进行萃取,需要几次振荡并放气,然后将分液漏斗置于铁架台的铁圈上静置 |
下列对于“塑料废弃物”的处理方法,最恰当的是( )
| A、将废弃物焚烧 |
| B、将废弃物填埋于土壤中 |
| C、将废弃物倾倒在海洋中 |
| D、将废弃物加工成防水材料或汽油,变废为宝 |