题目内容
(16分)(1)乙醇是重要的有机化工原料,可由乙烯直接水合法生产。
已知:甲醇脱水反应①2CH3OH(g) = CH3OCH3(g)+H2O(g)?△H1=-23.9KJ·mol-1
甲醇制烯烃反应②2CH3OH(g) = C2H4 (g)+2H2O(g)?△H2=-29.1KJ·mol-1
乙醇异构化反应③CH3CH2OH(g) = CH3OCH3(g))? △H3=+50.7KJ·mol-1
则乙烯气相直接水合反应C2H4 (g)+H2O(g) C2H5OH(g) △H= ;
C2H5OH(g) △H= ;
(2)乙烯气相直接水合反应,在其他条件相同时,分别测得C2H4的平衡转化率在不同压强(P1、P2)下随温度变化的曲线如下图。结合曲线归纳平衡转化率-T曲线变化规律:
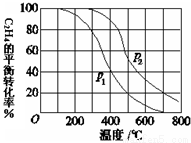
(a) ;
(b) ;
(3)若要进一步提高乙烯的转化率,可以采取的措施有 。
A.增大乙烯的浓度 B.分离出乙醇 C.加催化剂
(4)已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.25。
Fe(s)+CO2(g)的平衡常数K=0.25。
①t℃时,反应达到平衡时n(CO):n(CO2)= 。
②若在1 L密闭容器中加入0.02 mol FeO(s),并通入x mol CO,t℃时反应达到平衡。此时FeO(s)转化率为50%,求x的值。(写出计算步骤)
(16分(1)-45.5 kJ·mol-1(2分,错写或漏写单位扣1分,数值错,0分)
(2)(a)其他条件相同,温度升高,C2H4的平衡转化率降低;(2分,合理给分)
(b)其他条件相同,增大压强, C2H4的平衡转化率增大。(2分,合理给分)
(3)B (2分) (4)①4:1 (2分) ②0.05
【解析】
试题分析:(1)已知:甲醇脱水反应 ①2CH3OH(g)═CH3OCH3(g)+H2O(g)△H1=-23.9kJ?mol-1、甲醇制烯烃反应 ②2CH3OH(g)═C2H4(g)+2H2O(g)△H2=-29.1kJ?mol-1、乙醇异构化反应 ③C2H5OH(g)═CH3OCH3(g)△H3=+50.7kJ?mol-1,根据盖斯定律①-②-③可得:C2H4(g)+H2O(g)═C2H5OH(g)△H=(-23.9+29.1-50.7)kJ/mol=-45.5kJ/mol;
(2)根据图像的变化曲线可知:(a)其他条件相同,温度升高,C2H4的平衡转化率降低;(b)其他条件相同,增大压强, C2H4的平衡转化率增大。
(3)A.增大乙烯的浓度,平衡向正反应方向碱性,但乙烯的转化率降低,A错误;B.分离出乙醇,降低生成物浓度,平衡向正反应方向碱性,乙烯转化率增大,B正确;C.加催化剂不能改变平衡状态,转化率不变,C错误,答案选B。
(4)①已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.25,则反应达到平衡时n(CO):n(CO2)=1/K=1/0.25=4:1;
Fe(s)+CO2(g)的平衡常数K=0.25,则反应达到平衡时n(CO):n(CO2)=1/K=1/0.25=4:1;
②FeO(s) + CO(g)  Fe(s) + CO2(g)
Fe(s) + CO2(g)
起始时物质的量(mol) 0.02 x 0 0
变化的物质的量(mol) 0.02×50% 0.01 0.01 0.01
平衡时物质的量(mol) 0.01 x-0.01 0.01 0.01
根据平衡常数K=0.25得:
解得x=0.05
考点:考查盖斯定律的应用、外界条件对平衡状态的影响以及平衡常数的应用与计算



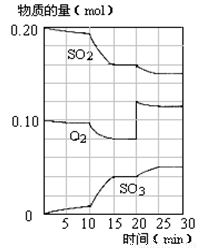
 2SO3
2SO3