题目内容
采用32%~35%的FeCl3溶液腐蚀印刷线路板上的金属铜,腐蚀废液中主要含有CuCl2、FeCl2和HCl等溶质.
(1)用FCl3溶液溶解印刷线路板上金属铜的离子方程式为 .
(2)工业上两种回收腐蚀废液中铜的方法如下:
①第一种:电解腐蚀废液回收铜.阳极(石墨)的电极反应可表示为 .
②第二种:用铁粉置换腐蚀废液中的铜.
用铁粉回收铜的实验操作为:加入过量铁粉,充分搅拌,过滤、 、 、 、 .
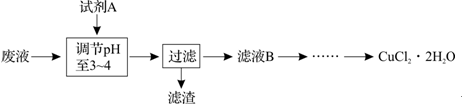
(3)工业上也可用腐蚀废液制备CuCl2?2H2O,从而进行对废液的利用,其工艺流程如下:
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
①试剂A最好应选用 (填写字母代号),理由是 .
a.浓硫酸 b.Cl2 c.NaClO d.NaOH溶液
②测定产品中CuCl2?2H2O的质量分数如下:取2.000g产品,用水溶解后,加入60.00mL 0.4000mol?L-1的KI溶液(足量),充分反应后加入淀粉指示剂,用0.4000mol?L-1 Na2S2O3标准溶液滴定,耗去此标准液25.00mL时,刚好到达滴定终点(已知:2Cu2++4I-=2CuI↓+I2,I2+2S2O32-=2I-+S4O62-).此产品中CuCl2?2H2O的质量分数为 (写出计过程).
(1)用FCl3溶液溶解印刷线路板上金属铜的离子方程式为
(2)工业上两种回收腐蚀废液中铜的方法如下:
①第一种:电解腐蚀废液回收铜.阳极(石墨)的电极反应可表示为
②第二种:用铁粉置换腐蚀废液中的铜.
用铁粉回收铜的实验操作为:加入过量铁粉,充分搅拌,过滤、
(3)工业上也可用腐蚀废液制备CuCl2?2H2O,从而进行对废液的利用,其工艺流程如下:

部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 4.7 |
| 完全沉淀 | 4.1 | 9.7 | 6.7 |
a.浓硫酸 b.Cl2 c.NaClO d.NaOH溶液
②测定产品中CuCl2?2H2O的质量分数如下:取2.000g产品,用水溶解后,加入60.00mL 0.4000mol?L-1的KI溶液(足量),充分反应后加入淀粉指示剂,用0.4000mol?L-1 Na2S2O3标准溶液滴定,耗去此标准液25.00mL时,刚好到达滴定终点(已知:2Cu2++4I-=2CuI↓+I2,I2+2S2O32-=2I-+S4O62-).此产品中CuCl2?2H2O的质量分数为
考点:铜金属及其重要化合物的主要性质,物质分离和提纯的方法和基本操作综合应用
专题:元素及其化合物
分析:(1)铜具有还原性,铁离子具有氧化性,二者之间发生氧化还原反应;
(2)金属铁可以和氯化铜反应置换出金属铜,剩余的铁可以和盐酸反应,但是金属铜和盐酸之间不反应;
(3)获得CuCl2?2H2O晶体,需要利用重结晶法把硫酸钠除掉,蒸发浓缩后,由于同温下硫酸钠的溶解度小,会有大量硫酸钠析出,故趁热过滤掉析出的硫酸钠;
根据反应的过程:2Cu2++4I-=2CuI↓+I2,I2+2S2O32-=2I-+S4O62-,得到关系式:Cu2+~S2O32-,进行计算即可.
(2)金属铁可以和氯化铜反应置换出金属铜,剩余的铁可以和盐酸反应,但是金属铜和盐酸之间不反应;
(3)获得CuCl2?2H2O晶体,需要利用重结晶法把硫酸钠除掉,蒸发浓缩后,由于同温下硫酸钠的溶解度小,会有大量硫酸钠析出,故趁热过滤掉析出的硫酸钠;
根据反应的过程:2Cu2++4I-=2CuI↓+I2,I2+2S2O32-=2I-+S4O62-,得到关系式:Cu2+~S2O32-,进行计算即可.
解答:
解:(1)铜具有还原性,铁离子具有氧化性,二者之间发生的氧化还原反应为:2FeCl3+Cu=2FeCl2+CuCl2,故答案为:2FeCl3+Cu=2FeCl2+CuCl2;
(2)①则阳极(石墨)上的电极发生氧化反应,Fe2+失去电子生成Fe3+,反应式为:Fe2+-e-═Fe3+,故答案为:Fe2+-e-═Fe3+;
②金属铁可以和氯化铜反应置换出金属铜,但是和氯化亚铁之间不反应,加入足量的金属铁,保证铜均被置换出来,剩余的铁可以和盐酸反应,但是金属铜和盐酸之间不反应,再过滤可以滤出金属铜,最后将铜干燥即可,故答案为:在滤渣中加入足量稀盐酸并搅拌;过滤;用适量蒸馏水洗涤滤渣;将滤渣干燥即得铜;
(3)①为了将废液中的亚铁离子除去,加入一种试剂将亚铁离子氧化为铁离子,调节pH值,可以将铁离子沉淀出来,但是铜离子不沉淀即可,故选NaClO,它具有碱性和氧化性,能将Fe2+氧化为Fe3+,且反应能消耗H+,增大溶液的pH使Fe3+沉淀,故答案为:c;①NaClO能将Fe2+氧化为Fe3+,且反应能消耗H+,增大溶液的pH使Fe3+沉淀;
②依据2Na2S2O3+I2═Na2S4O6+2NaI,2Cu2++4I-=2CuI↓+I2;
得到 Na2S2O3~Cu2+
1 1
0.4000mol/L×0.0250L 0.01mol
则CuCl2?2H2O的物质的量为:0.01mol,
试样中CuCl2?2H2O的质量百分数为
×100%=85.50%.
故答案为:85.50%.
(2)①则阳极(石墨)上的电极发生氧化反应,Fe2+失去电子生成Fe3+,反应式为:Fe2+-e-═Fe3+,故答案为:Fe2+-e-═Fe3+;
②金属铁可以和氯化铜反应置换出金属铜,但是和氯化亚铁之间不反应,加入足量的金属铁,保证铜均被置换出来,剩余的铁可以和盐酸反应,但是金属铜和盐酸之间不反应,再过滤可以滤出金属铜,最后将铜干燥即可,故答案为:在滤渣中加入足量稀盐酸并搅拌;过滤;用适量蒸馏水洗涤滤渣;将滤渣干燥即得铜;
(3)①为了将废液中的亚铁离子除去,加入一种试剂将亚铁离子氧化为铁离子,调节pH值,可以将铁离子沉淀出来,但是铜离子不沉淀即可,故选NaClO,它具有碱性和氧化性,能将Fe2+氧化为Fe3+,且反应能消耗H+,增大溶液的pH使Fe3+沉淀,故答案为:c;①NaClO能将Fe2+氧化为Fe3+,且反应能消耗H+,增大溶液的pH使Fe3+沉淀;
②依据2Na2S2O3+I2═Na2S4O6+2NaI,2Cu2++4I-=2CuI↓+I2;
得到 Na2S2O3~Cu2+
1 1
0.4000mol/L×0.0250L 0.01mol
则CuCl2?2H2O的物质的量为:0.01mol,
试样中CuCl2?2H2O的质量百分数为
| 0.01mol×171g/mol |
| 2.0g |
故答案为:85.50%.
点评:本题以实验的方法考查学生含铁化合物的性质知识,注重物质的分离、提纯和化学实验基本操作的知识以及根据化学方程式进行计算的知识,难度中等.

练习册系列答案
相关题目
据报道,摩托罗拉公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.已知电池的总反应式为:2CH3OH+3O2+4KOH
2K2CO3+6H2O则下列说法正确的是( )
| 放电 |
| 充电 |
| A、构成该电池的正极和负极必须是两种活性不同的金属 |
| B、放电时CH3OH为电池的正极 |
| C、放电时每消耗1 mol CH3OH转移12mol电子 |
| D、放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
如图所示,y表示沉淀的量,x表示加试剂的体积,能够用该图表示的反应是( )


| A、向Ca(OH)2溶液中通人CO2至过量 |
| B、在盐酸和硫酸的混合溶液中加入Ba(OH)2溶液至过量 |
| C、在水玻璃和烧碱混合溶液中加入盐酸至过量 |
| D、在Ba(OH)2溶液中加入氯化铝溶液至过量 |
实验室中,欲除去食盐水中的水,须选用( )
| A、烧杯 | B、蒸发皿 |
| C、分液漏斗 | D、表面皿 |
下列说法中正确的是( )
| A、二氧化硫溶于水能导电,故二氧化硫属于电解质 |
| B、铜可以导电,故铜是电解质 |
| C、硫酸钡难溶于水,故硫酸钡属于弱电解质 |
| D、氢离子浓度相同的盐酸和醋酸导电能力相同 |
下列关于氧化铝的说法中,不正确的是( )
| A、难溶于水 |
| B、能与盐酸反应 |
| C、能与NaOH溶液反应 |
| D、能与铁反应生成铝 |
下列说法正确的是( )
| A、pH<7的溶液一定是酸性溶液 |
| B、改变外界条件使溶液中c(H+)增大,则其pH增大 |
| C、室温下,每1×107个水分子中只有一个水分子发生电离 |
| D、常温时,pH=5的溶液和pH=3的溶液相比,前者c(OH-)是后者的100倍 |
下列离子方程式书写正确的是( )
| A、石灰水中通入少量CO2:Ca2++2OH-+CO2=CaCO3↓+H2O |
| B、稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、将金属钠加入水中:Na+2H2O=Na++2OH-+H2↑ |
| D、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
 (1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是
(1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是