题目内容
10.下列根据实验操作和现象所得到的结论正确的是.| 选项 | 试验操作和现象 | 结论 |
| A | 向浓度均为0.1mol.L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液,先出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| B | 向滴有甲基橙的AgNO3溶液中滴加KCl溶液,溶液由红色变为黄色 | KCl溶液具有碱性 |
| C | 室温下,实验测得:0.1mol.L-1Na2CO3溶液的PH约为11.6;0.1mol.L-1NaHCO3溶液的PH约为7.9 | CO32-结合H+的能力比HCO3-的强 |
| D | 某盐酸溶液中滴加盐酸,产生无色无味气体,将气体通入澄清石灰水变浑浊 | 该盐一定是碳酸盐 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.滴加少量AgNO3溶液,Ksp小的先沉淀;
B.反应生成AgCl和硝酸钾,pH增大,KCl为强酸强碱盐;
C.等浓度时pH越大,可知水解程度越大;
D.碳酸盐、碳酸氢盐均与盐酸反应生成二氧化碳.
解答 解:A.滴加少量AgNO3溶液,Ksp小的先沉淀,由现象可知先生成AgI,则Ksp(AgCl)>Ksp(AgI),故A错误;
B.反应生成AgCl和硝酸钾,pH增大,KCl为强酸强碱盐,KCl溶液为中性,故B错误;
C.等浓度时pH越大,可知水解程度越大,则CO32-结合H+的能力比HCO3-的强,故C正确;
D.碳酸盐、碳酸氢盐均与盐酸反应生成二氧化碳,则该盐可能为碳酸盐,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握沉淀的生成、盐类水解、物质的检验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
1.事实上,许多氧化物在一定条件下能与Na2O2反应,且反应极有规律,如Na2O2+SO2═Na2SO4,2Na2O2+2SO3═2Na2SO4+O2,据此你认为下列反应方程式中不正确的是( )
| A. | 2Na2O2+2N2O5═4NaNO3+O2↑ | B. | Na2O2+2NO2═2NaNO2+O2 | ||
| C. | Na2O2+N2O4═2NaNO3 | D. | 2Na2O2+2Mn2O7═4NaMnO4+O2↑ |
18.化学与生活、社会密切相关.下列说法正确的是( )
| A. | 合成酚醛树脂的单体是苯酚和甲醇 | |
| B. | 汽油和乙烯均为石油分馏得到的产品 | |
| C. | 塑料、合成纤维和合成橡胶都属于合成材料 | |
| D. | 蔗糖、淀粉、油脂水解均能生成电解质 |
5.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | KW/C(OH-)=10-12mol•L-1的溶液中:Na+、K+、SiO32-、Cl- | |
| B. | 使甲基橙变黄的溶液中:NH4+、Cu2+、NO3-、SO42- | |
| C. | 由水电离出的 c(H+ )=1.0×l0-13 mol•L-1的溶液中:Na+、CO32-、SO32-、Cl- | |
| D. | 使KSCN显红色的溶液中:NH4+、K+、Cl-、A1O2- |
19.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙呈红色的溶液中:K+、Ba2+、OH-、AlO2- | |
| B. | 由水电离出C(H+)=1×10-14溶液中:Ca2+、K+、Cl-、HCO3- | |
| C. | $\frac{C({H}^{+})}{C(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | C(Fe3+)=0.1mol/L的溶液中:K+、CO32-、SO42-、SCN- |
20. 实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,回答下列问题:
实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,回答下列问题:
(1)已知在一定温度下,
①C(s)+CO2(g)?2CO(g)△H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3 平衡常数K3.
则K1、K2、K3之间的关系是:K3=K1×K2,△H3=(a+b) kJ/mol(用含a、b的代数式表示).
(2)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
该反应的正反应方向是放热反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol•L-1,在该条件下,CO的平衡转化率为:75%.
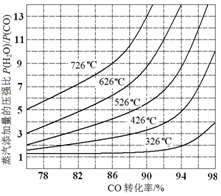
(3)在催化剂存在条件下反应:H2O(g)+CO(g)?CO2(g)+H2(g),CO转化率随蒸气添加量的压强比及温度变化关系如图所示:
对于气相反应,用某组分(B)的平衡分压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=$\frac{P(C{O}_{2})•P({H}_{2})}{P(CO)•P({H}_{2}O)}$.
 实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,回答下列问题:
实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,回答下列问题:(1)已知在一定温度下,
①C(s)+CO2(g)?2CO(g)△H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3 平衡常数K3.
则K1、K2、K3之间的关系是:K3=K1×K2,△H3=(a+b) kJ/mol(用含a、b的代数式表示).
(2)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(3)在催化剂存在条件下反应:H2O(g)+CO(g)?CO2(g)+H2(g),CO转化率随蒸气添加量的压强比及温度变化关系如图所示:
对于气相反应,用某组分(B)的平衡分压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=$\frac{P(C{O}_{2})•P({H}_{2})}{P(CO)•P({H}_{2}O)}$.
 根据所学知识完成下列填空.
根据所学知识完成下列填空.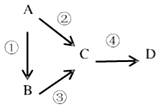 A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如下转化关系,其中A是单质.
A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如下转化关系,其中A是单质.