题目内容
16.怎样除去氯化钠中少量的硝酸钾?怎样除去硝酸钾中少量的氯化钠?在结晶操作中,一般将需要提纯的物质结晶出来还是将杂质结晶出?为什么?分析 硝酸钾的溶解度较大,且随温度变化较大,可用结晶法分离,一般方法为蒸发结晶或冷却结晶,以此解答.
解答 解:硝酸钾的溶解度较大,且随温度变化较大,除去氯化钠中少量的硝酸钾,可用蒸发结晶的方法,而除去硝酸钾中少量的氯化钠,可用冷却热饱和溶液的方法,在结晶操作中,一般将需要提纯的物质结晶出来,因被提纯的物质不可能完全结晶,可少量存在母液中,
答:用蒸发结晶的方法除去氯化钠中少量的硝酸钾,用冷却结晶的方法除去硝酸钾中少量的氯化钠,因被提纯的物质不可能完全结晶,可少量存在母液中,在结晶操作中,一般将需要提纯的物质结晶出来.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
| A. | C16H25O5 | B. | C14H16O4 | C. | C14H18O5 | D. | C16H25O5 |
11.利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 项 | ① | ② | ③ | 实验结论 | 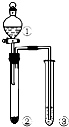 |
| A | 稀盐酸 | Na2SO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si | |
| B | 稀硫酸 | Na2S | 滴加少量AgNO3的KI溶液 | Ksp(AgI)>Ksp(Ag2S) | |
| C | 浓盐酸 | KMnO4 | AgNO3和稀硝酸混合溶液 | Cl2溶于水有Cl-生成 | |
| D | 浓硫酸 | 蔗糖 | Ba(OH)2溶液 | SO2能与碱溶液反应 |
| A. | A | B. | B | C. | C | D. | D |
1.下列有关离子反应的判断正确的是( )
| A. | 2Fe3++Fe═3Fe2+成立,说明氧化性:Fe3+>Fe2+ | |
| B. | SO2饱和溶液中NH4+、K+、CO32-、SO32-可大量存在 | |
| C. | 用NaOH溶液吸收尾气中的氯气:Cl2+4OH-═2ClO-+2H2O | |
| D. | 向NaHS溶液中加入适量硝酸发生反应:HS-+H+═H2S↑ |
8.下列物质中属于纯净物的是( )
| A. | 液氯 | B. | 普通玻璃 | C. | 漂白粉 | D. | 水泥 |
5.下列对CH2Cl2的叙述中不正确的是( )
| A. | 无同分异构体 | B. | 有两种同分异构体 | ||
| C. | 常温常压下为液态 | D. | 不是正四面体结构 |
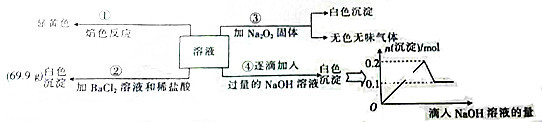
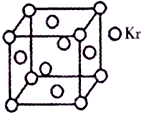 我国部分城市灰霾天占全年一半.引起灰霾的PM2.5微细粒子包含(NH4)2S04、NH4N03、有机颗粒物及扬尘等.通过测定灰霾中锌等重金属的含量,可知交通污染是目前造成我国灰霾天气主要原因之一.
我国部分城市灰霾天占全年一半.引起灰霾的PM2.5微细粒子包含(NH4)2S04、NH4N03、有机颗粒物及扬尘等.通过测定灰霾中锌等重金属的含量,可知交通污染是目前造成我国灰霾天气主要原因之一.