题目内容
14.(1)相同反应物,滴加顺序不同,离子方程式不同,如:在AlCl3溶液中滴入几滴NaOH溶液,离子方程式为Al3++3OH-═Al(OH)3↓.在NaOH溶液中滴入几滴AlCl3溶液,离子方程式为Al3++4OH-═AlO2-+2H2O.(2)微溶物状态不同,离子方程式不同,如:石灰乳与Na2CO3溶液反应的离子方程式为Ca(OH)2+CO32-═CaCO3↓+2OH-.澄清石灰水与Na2CO3溶液反应的离子方程式为Ca2++CO32-═CaCO3↓.
(3)将一小片铜片加入稀硫酸中没有反应,再加入适量KNO3晶体,则铜片逐渐溶解,并产生无色气体.3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O.
(4)向氢氧化钡溶液中滴加明矾溶液至Ba2+完全沉淀,离子方程式为:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O,继续加入明矾溶液,又发生的反应离子方程式为:Al3++3AlO2-+6H2O═4Al(OH)3↓.
(5)已知Br2水与FeCl2(aq)发生如下反应:3Br2+6FeCl2═4FeCl3+2FeBr3现将112mL(标准状况)Cl2通入10.0mL 1.0mol/L的FeBr2(aq)中,写出发生反应的离子方程式2Fe2++Cl2═2Fe3++2Cl-.
分析 (1)在AlCl3溶液中滴入几滴NaOH溶液,反应生成氢氧化铝和氯化钠;在NaOH溶液中滴入几滴AlCl3溶液,反应生成偏铝酸钠和水;
(2)石灰乳在离子反应中保留化学式,反应生成碳酸钙和NaOH;澄清石灰水与Na2CO3溶液反应,反应生成碳酸钙、NaOH;
(3)发生氧化还原反应生成铜离子、NO和水;
(4)向氢氧化钡溶液中滴加明矾溶液至Ba2+完全沉淀,反应生成硫酸钡、偏铝酸钾;继续加入明矾溶液,铝离子与偏铝酸根离子相互促进水解生成氢氧化铝沉淀;
(5)112mL(标准状况)Cl2通入10.0mL 1.0mol/L的FeBr2(aq)中,n(Cl2)=0.005mol,n(FeBr2)=0.01mol,由电子守恒可知,只有亚铁离子被氧化.
解答 解:(1)在AlCl3溶液中滴入几滴NaOH溶液,反应生成氢氧化铝和氯化钠,离子反应为Al3++3OH-═Al(OH)3↓;在NaOH溶液中滴入几滴AlCl3溶液,反应生成偏铝酸钠和水,离子反应为Al3++4OH-═AlO2-+2H2O,
故答案为:Al3++3OH-═Al(OH)3↓;Al3++4OH-═AlO2-+2H2O;
(2)石灰乳在离子反应中保留化学式,反应生成碳酸钙和NaOH,离子反应为Ca(OH)2+CO32-═CaCO3↓+2OH-;澄清石灰水与Na2CO3溶液反应,反应生成碳酸钙、NaOH,离子反应为Ca2++CO32-═CaCO3↓,
故答案为:Ca(OH)2+CO32-═CaCO3↓+2OH-;Ca2++CO32-═CaCO3↓;
(3)发生氧化还原反应生成铜离子、NO和水,离子反应为3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O,故答案为:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O;
(4)向氢氧化钡溶液中滴加明矾溶液至Ba2+完全沉淀,反应生成硫酸钡、偏铝酸钾,离子反应为2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O;继续加入明矾溶液,铝离子与偏铝酸根离子相互促进水解生成氢氧化铝沉淀,离子反应为Al3++3AlO2-+6H2O═4Al(OH)3↓,
故答案为:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O;Al3++3AlO2-+6H2O═4Al(OH)3↓;
(5)112mL(标准状况)Cl2通入10.0mL 1.0mol/L的FeBr2(aq)中,n(Cl2)=0.005mol,n(FeBr2)=0.01mol,由电子守恒可知,只有亚铁离子被氧化,离子反应为2Fe2++Cl2═2Fe3++2Cl-,故答案为:2Fe2++Cl2═2Fe3++2Cl-.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电荷守恒,题目难度不大.

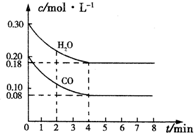 (1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,
(1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1,850℃时,此反应的平衡常数为1,CO的转化率为60%.
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表:
| t/min | c(CO)/mol•L-1 | c(H2O)/mol•L-1 | c(CO2)/mol•L-1 | c(H2)/mol•L-1 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②反应在4~5min间,平衡向逆反应方向移动,可能的原因是c,表中5~6min之间数值发生变化,可能的原因是b.
a.降低温度b.增加水蒸气 c.增加氢气浓度d.使用催化剂.
| A. | 酸性氧化物不一定能与水反应生成对应的酸,与水反应生成酸的氧化物不一定是酸性氧化物 | |
| B. | 碱性氧化物不一定能与水反应生成对应的碱,与水反应生成碱的氧化物不一定是碱性氧化物 | |
| C. | SO2、Na2O的水溶液都能导电,所以它们都是电解质 | |
| D. | 在溶于水或熔融状态下能够自身发生电离的化合物一定是电解质 |
| A. | 植物油 | B. | 电石 | C. | 棉被、衣物 | D. | 过氧化钠 |
| A. | Na2O2 | B. | H3O+ | C. | NH4Cl | D. | NaOH |
| A. | 水在高温加热后变成水蒸气 | B. | 生石灰变熟石灰 | ||
| C. | 石墨转变为金刚石 | D. | 钠投入水中 |
| A. | Fe2O3 | B. | HCl | C. | ZnSO4 | D. | FeSO4 |