题目内容
2.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )| A. | 1mol甲醇中含有C-H键的数目为4NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 标准状况下,2.24L己烷含有分子的数目为0.1NA | |
| D. | 1mol甲基所含的电子数目为9NA |
分析 A、甲醇的结构简式为CH3OH;
B、溶液体积不明确;
C、标况下己烷为液体;
D、甲基中含9个电子.
解答 解:A、甲醇的结构简式为CH3OH,故1mol甲醇中含3NA个C-H键,故A错误;
B、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故B错误;
C、标况下己烷为液体,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、甲基中含9个电子,故1mol甲基中含9NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案
相关题目
12.下列元素的基态原子中最难失去电子的是( )
| A. | F | B. | O | C. | Ne | D. | He |
13.铁镍蓄电池又称爱迪生电池.放电时的总反应为:Fe+Ni2O3+3H2O═Fe(OH)2+2Ni(OH)2.下列有关该电池的说法错误的是( )
| A. | 电池的电解液为碱性溶液,负极为Fe | |
| B. | 电池放电时,负极反应为Fe+2OH--2e-═Fe(OH)2 | |
| C. | 电池充电过程中,阴极附近溶液的pH减小 | |
| D. | 电池充电时,OH-向阳极迁移 |
7.下列说法或表示方法中,正确的是( )


| A. | 等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量少 | |
| B. | 如图可表示C和H2O(g)反应过程中的能量变化 | |
| C. | 吸热反应一定要加热,才能进行 | |
| D. | 已知中和热为57.3 kJ•mol-1,则浓硫酸与NaOH溶液反应生成 1mol H2O时,共放出57.3 kJ的能量 |
11.某烃的分子组成是苯环上2个互为对位的碳原子上连接有2个丁基,结构可以表示为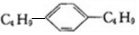 ,符合这一结构的烃有( )
,符合这一结构的烃有( )
 ,符合这一结构的烃有( )
,符合这一结构的烃有( )| A. | 16种 | B. | 12种 | C. | 8种 | D. | 10种 |
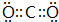 ,B与D形成的原子个数比为1:1的化合物的电子式是
,B与D形成的原子个数比为1:1的化合物的电子式是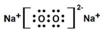 .
.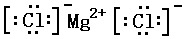 ; ②NaOH
; ②NaOH ;
;