题目内容
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、1molCl2参加的任何反应,反应过程中转移电子数都是2NA | ||
| B、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | ||
C、标准状况下,1L乙醇完全燃烧产生CO2分子的数目为
| ||
| D、将10mL质量分数为98%的浓H2SO4,用水稀释至100mL,H2SO4的质量分数大于9.8% |
考点:阿伏加德罗常数
专题:
分析:A、氯气参与的反应转移的电子的物质的量取决于反应后氯元素的价态;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、标况下,乙醇是液态;
D、稀释以后,硫酸溶液的密度变小,m(100ml硫酸)<10×m(10ml硫酸),而溶质硫酸的质量不变;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、标况下,乙醇是液态;
D、稀释以后,硫酸溶液的密度变小,m(100ml硫酸)<10×m(10ml硫酸),而溶质硫酸的质量不变;
解答:
解:A、氯气参与的反应转移的电子的物质的量取决于反应后氯元素的价态,故1molCl2参加的反应,反应过程中转移电子数不一定是2NA,故A错误;
B、常温常压下,气体摩尔体积大于22.4L/mol,即33.6L氯气的物质的量小于1.5mol,与27g铝即1mol铝反应时铝过量,故转移的电子数小于3NA,故B错误;
C、标况下,乙醇是液态,故C错误;
D、由于稀释以后,硫酸溶液的密度变小,m(100ml硫酸)<10×m(10ml硫酸),而溶质硫酸的质量不变,故质量分数大于9.8%,故D正确.
故选D.
B、常温常压下,气体摩尔体积大于22.4L/mol,即33.6L氯气的物质的量小于1.5mol,与27g铝即1mol铝反应时铝过量,故转移的电子数小于3NA,故B错误;
C、标况下,乙醇是液态,故C错误;
D、由于稀释以后,硫酸溶液的密度变小,m(100ml硫酸)<10×m(10ml硫酸),而溶质硫酸的质量不变,故质量分数大于9.8%,故D正确.
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
下列各组离子能在水溶液中大量共存的是( )
| A、H+、Fe2+、ClO-、SO42- |
| B、Na+、Cu2+、S2-、ClO- |
| C、Na+、Ba2+、OH-、NO3- |
| D、Na+、Al3+、SiO32-、CO32- |
下列说法正确的是( )
| A、所有元素中原子半径最小的是F |
B、根据π键的成键特征判断C-C的键能与  键能的关系是双键的键能小于单键的键能的2倍 键能的关系是双键的键能小于单键的键能的2倍 |
| C、元素电负性越小,元素非金属性越强 |
| D、第n周期第n主族的元素均为金属 |
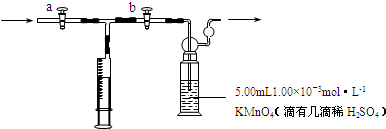
 合肥市某校化学兴趣小组为探究铁与浓硫酸反应,设计了如图所示装置进行实验.
合肥市某校化学兴趣小组为探究铁与浓硫酸反应,设计了如图所示装置进行实验.
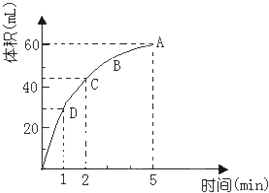 为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50mL密度为1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示.请依图回答下列问题:
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50mL密度为1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示.请依图回答下列问题: A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显红色,它们相互转化关系如图所示.
A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显红色,它们相互转化关系如图所示.