题目内容
加热A2B5气体按下式分解:
A2B5(g)?A2B3(g)+B2(g) ①
A2B3(g)?A2B+B2(g) ②
在容积为2L的密闭容器中将4mol A2B3加热至t℃,达到平衡后,B2浓度为0.5mol?L-1,A2B5浓度为0.7mol?L-1,则t℃时A2B3的平衡浓度是( )
A2B5(g)?A2B3(g)+B2(g) ①
A2B3(g)?A2B+B2(g) ②
在容积为2L的密闭容器中将4mol A2B3加热至t℃,达到平衡后,B2浓度为0.5mol?L-1,A2B5浓度为0.7mol?L-1,则t℃时A2B3的平衡浓度是( )
| A、1.5 mol?L-1 |
| B、0.2 mol?L-1 |
| C、0.1 mol?L-1 |
| D、0.9 mol?L-1 |
考点:化学平衡的计算
专题:化学平衡专题
分析:应用原子守恒法,初始时存在的物质是A2B3,分别计算出A、B的物质的量,列方程组解答.
解答:
解:初始时存在的物质是A2B3,A的物质的量是4mol×2=8mol,B的物质的量是4mol×3=12mol;
反应平衡后,存在的物质是A2B5,A2B3,A2B和B2,根据它们的浓度和容器容积可以分别算出它们中含A和B元素的物质的量(假设A2B3浓度为x mol/L,A2B的浓度为y mol/L)如下所示:
物质:A2B5 A2B3 A2B B2
浓度:0.7mol/L x mol/L y mol/L 0.5mol/L
物质的量:1.4mol 2x mol 2y mol 1mol
A物质的量:2.8mol 4x mol 4y mol 0mol
B物质的量:7mol 6x mol 2y mol 2mol
根据A原子物质的量反应前后相等(即A原子总数不变,原子守恒),得
2.8+4x+4y+0=8mol
根据B原子物质的量反应前后相等(即B原子总数不变,原子守恒),得
7+6x+2y+2=12mol
解方程组得:x=0.1 mol/L,y=1.2 mol/L
故选C.
反应平衡后,存在的物质是A2B5,A2B3,A2B和B2,根据它们的浓度和容器容积可以分别算出它们中含A和B元素的物质的量(假设A2B3浓度为x mol/L,A2B的浓度为y mol/L)如下所示:
物质:A2B5 A2B3 A2B B2
浓度:0.7mol/L x mol/L y mol/L 0.5mol/L
物质的量:1.4mol 2x mol 2y mol 1mol
A物质的量:2.8mol 4x mol 4y mol 0mol
B物质的量:7mol 6x mol 2y mol 2mol
根据A原子物质的量反应前后相等(即A原子总数不变,原子守恒),得
2.8+4x+4y+0=8mol
根据B原子物质的量反应前后相等(即B原子总数不变,原子守恒),得
7+6x+2y+2=12mol
解方程组得:x=0.1 mol/L,y=1.2 mol/L
故选C.
点评:本题考查化学平衡的有关计算,利用原子守恒法解题方便.

练习册系列答案
相关题目
2mol A与2mol B混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g)?2C(g)+zD(g),若2s后,A的转化率为50%,测得v(D)=0.25mol?L-1?s-1,下列推断正确的是( )
| A、v(B)=0.75 mol?L-1?s-1 |
| B、z=2 |
| C、B的转化率为25% |
| D、C的体积分数约为28.6% |
下列说法正确的是( )
| A、同周期元素的第一电离能从左往右越来越大 |
| B、同主族元素从上到下第一电离能越来越大 |
| C、同周期元素的电负性从左往右越来越大 |
| D、同主族元素从上到下电负性越来越大 |
将3mol CO和2.5mol H2O的混合气体充入容积为2L的密闭容器内,发生反应:
CO(g)+H2O(g)
CO2(g)+H2(g),5min后生成0.75mol?L-1的CO2.下列说法正确的是( )
CO(g)+H2O(g)
| 催化剂 |
| 高温 |
| A、CO的平均消耗速率为0.3 mol?L-1?min-1 |
| B、5 min后,气体的总物质的量浓度为2mol?L-1 |
| C、若单位时间内生成H2和H2O的物质的量之比为1:1,则体系处于平衡状态 |
| D、平衡后,增大压强,平衡将向正反应方向移动 |
将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物全部是NO).向反应后的溶液中加入1.5mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列叙述中正确的是( )
| A、当生成沉淀达到最大值时,消耗NaOH溶液的体积小于200mL |
| B、当金属全部溶解时收集到NO气体的体积标准状况下为2.24L |
| C、参加反应的金属的总质量一定是6.6g |
| D、当金属全部溶解时,参加反应的硝酸的物质的量是0.3mol |
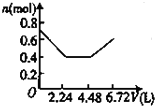

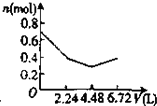

 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题.
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题. 在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应: