题目内容
下列实验方案设计合理且能达到相应实验预期目的是( )
A、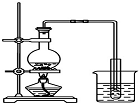 制取少量蒸馏水 |
B、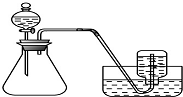 用铜和浓硝酸制取少量NO2 |
C、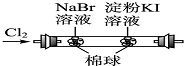 证明氧化性:Cl2>Br2>I2 |
D、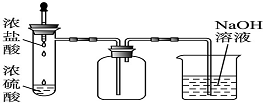 制取HCL且除去多余的气体 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.利用蒸馏原理来制取蒸馏水;
B.二氧化氮能与水反应,不能利用排水法收集;
C.氯气能与碘化钾反应;
D.导管不能插入液面下.
B.二氧化氮能与水反应,不能利用排水法收集;
C.氯气能与碘化钾反应;
D.导管不能插入液面下.
解答:
解:A.图中为蒸馏装置,可利用蒸馏原理来制取蒸馏水,故A正确;
B.二氧化氮能与水反应,不能利用排水法收集,图中收集装置错误,故B错误;
C.氯气能与碘化钾反应,应将溴单质中的氯气除掉,故C错误;
D.导管不能插入液面下,以免发生倒吸,故D错误;
故选A.
B.二氧化氮能与水反应,不能利用排水法收集,图中收集装置错误,故B错误;
C.氯气能与碘化钾反应,应将溴单质中的氯气除掉,故C错误;
D.导管不能插入液面下,以免发生倒吸,故D错误;
故选A.
点评:本题考查化学实验方案的评价,涉及蒸馏、气体的制取及收集、氧化性的比较、气体制取的实验,侧重实验细节的考查,题目难度不大.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
设NA为阿佛加德罗常数,下列说法正确的是( )
①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1L 2mol/L的氯化镁溶液中含氯离子为4NA
④标准状况下22.4LH2O中分子数为NA
⑤在同温同体积时,气体物质的物质的量越大,则压强越大;
⑥同温同压下,气体的密度与气体的相对分子质量成正比.
①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1L 2mol/L的氯化镁溶液中含氯离子为4NA
④标准状况下22.4LH2O中分子数为NA
⑤在同温同体积时,气体物质的物质的量越大,则压强越大;
⑥同温同压下,气体的密度与气体的相对分子质量成正比.
| A、①②③④ | B、③④⑥ |
| C、①③④ | D、①②③⑤⑥ |
下表为六种短周期元素的部分性质:下列有关说法错误的是( )
| 元素代号 | X | Y | Z | Q | R | T |
| 原子半径/10-10m | 0.77 | 0.74 | 0.75 | 1.17 | 0.99 | 1.10 |
| 主要化合价 | +4、-4 | -2 | +5、-3 | +4、-4 | +7、-1 | +5、-3 |
| A、X与Y可以形成阴离子XY32- |
| B、元素R的含氧酸一定为强酸 |
| C、Z的氢化物的沸点比T的氢化物的沸点高 |
| D、由X形成的化合物QX和XR4,其晶体类型不相同 |
下列各溶液中,一定能大量共存的是( )
| A、Fe3+、Na+、SO42-、H2O2 |
| B、C2H5OH、MnO4-、H+、K+ |
| C、Pb2+、K+、SO42-、Cl- |
| D、Na+、SO32-、CH3COO-、S2- |
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s)?NH3(g)+HI(g)②2HI(g)?H2(g)+I2(g),达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则此温度下NH3的平衡浓度为( )
①NH4I(s)?NH3(g)+HI(g)②2HI(g)?H2(g)+I2(g),达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则此温度下NH3的平衡浓度为( )
| A、0.5 | B、1 | C、4 | D、5 |
下面关于金属钠的描述正确的是( )
| A、钠的化学性质很活泼,钠离子和钠原子都具有较强的还原性 |
| B、钠能把钛锆等金属从它们的盐溶液中还原出来 |
| C、钠与氧气反应的产物与反应条件有关 |
| D、钠和钾的合金在室温下呈固态,可作原子反应堆的导热剂 |
下列有关活化分子的说法正确的是( )
| A、增大反应物浓度可以提高活化分子百分数 |
| B、升高温度能提高活化分子百分数 |
| C、使用合适的催化剂可以增大活化分子的能量 |
| D、增大体系的压强一定能提高活化分子百分数 |
下列每组内的物质,按单质、化合物、混合物顺序排列的是( )
| A、冰、生石灰、天然气 |
| B、碘酒、纯碱、胆矾 |
| C、金刚石、烧碱、纯盐酸 |
| D、液态氧、食醋、沼气 |
能说明醋酸是弱电解质的事实是( )
| A、醋酸溶液的导电性比盐酸弱 |
| B、醋酸溶液与碳酸钙反应,缓慢放出二氧化碳 |
| C、0.1mol L-1的CH3COOH溶液中氢离子浓度约为0.001 mol L-1 |
| D、醋酸溶液用水稀释后,氢离子浓度下降 |