题目内容
2.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/L的硫酸溶液中,乙同学将电极放入6mol/L的NaOH溶液中,实验装置如图所示:
(1)写出甲中正极的电极反应式:2H++2e-=H2↑.
(2)写出乙中负极的电极反应式:Al+4OH--3e-=AlO2-+2H2O,
总反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)如果甲、乙两同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应该比构成正极材料的金属活泼”,则甲会判断出Mg(填元素符号,下同)的活动性强,乙会判断出Al的活动性强.
(4)由此实验可知下列说法中正确的是ADE
A、利用原电池反应判断金属活动性顺序时,应注意介质的选择;
B、镁的金属性不一定比铝强;
C、该实验说明金属活动性顺序表已过时,没有实用价值;
D、该实验说明化学研究对象复杂,反应受条件影响大,应具体问题具体分析.
E、上述实验也反过来证明了“直接利用金属活动性顺序表判断电池的正负极”的这种说法不可靠.
(5)将乙装置设计为甲烷燃料电池,两极改为惰性电极,则负极反应式为CH4+10OH--8e-=CO32-+7H2O.
分析 甲同学依据的化学反应原理是Mg+H2SO4=MgSO4+H2↑,乙同学依据的化学反应原理是2Al+2NaOH+2H2O=2NaAlO2+3H2↑.由于Al显两性,与酸碱都能发生反应,(1)甲中镁易失电子作负极、Al作正极,负极上镁发生氧化反应、正极上氢离子发生还原反应;
(2)乙池中铝易失电子作负极、镁作正极,负极上铝失电子发生氧化反应;
(3)根据作负极的金属活泼性强结合电池中的负极判断;
(4)A.原电池正负极与电解质溶液有关;
B.镁的金属性大于铝;
C.该实验证明说明电解质溶液性质选用选择合适的介质,不能说明金属活动性顺序过时;
D.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
E、上述实验说明,“直接利用金属活动性顺序表判断电池中的正负极”并不考可靠,最好是接一个电流计,通过观察电流方向判断原电池的正负极;
(5)甲烷燃料电池以NaOH溶液为电解质溶液时,负极上是甲烷发生失电子的氧化反应,又因为电解质是NaOH溶液,二氧化碳和氢氧化钾反应得到的是碳酸钾,即CH4+10OH--8e-=CO32-+7H2O.
解答 解:(1)甲中镁易失电子作负极、Al作正极,负极上镁发生氧化反应、正极上氢离子发生还原反应,负极反应为Mg-2e-=Mg2+,正极反应为2H++2e-=H2↑,
故答案为:2H++2e-=H2↑;
(2)乙池中铝易失电子作负极,负极上铝失电子发生氧化反应,电极反应式为:Al+4OH--3e-=AlO2-+2H2O,镁作正极,正极发生还原反应,总反应为2Al+2OH-+2H2O=AlO2-+3H2↑,
故答案为:Al+4OH--3e-=AlO2-+2H2O;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)甲中镁作负极、乙中铝作负极,根据作负极的金属活泼性强判断,甲中镁活动性强、乙中铝活动性强,
故答案为:Mg;Al;
(4)A.根据甲、乙中电极反应式知,原电池正负极与电解质溶液有关,故A正确;
B.镁的金属性大于铝,但失电子难易程度与电解质溶液有关,故B错误;
C.该实验说明电解质溶液性质影响电极的正负极,不能说明金属活动性顺序没有使用价值,故C错误;
D.该实验说明化学研究对象复杂,反应与条件有关,电极材料相同其反应条件不同导致其产物不同,所以应具体问题具体分析,故D正确;
E.上述实验说明,“直接利用金属活动性顺序表判断电池中的正负极”并不考可靠,最好是接一个电流计,通过观察电流方向判断原电池的正负极,故E正确;
故答案为:ADE;
(5)甲烷燃料电池以NaOH溶液为电解质溶液时,负极上是甲烷发生失电子的氧化反应,又因为电解质是NaOH溶液,二氧化碳和氢氧化钾反应得到的是碳酸钾,即CH4+10OH--8e-=CO32-+7H2O,故答案为:CH4+10OH--8e-=CO32-+7H2O.
点评 本题考查了探究原电池原理,题目难度中等,明确原电池中各个电极上发生的反应是解本题关键,注意不能根据金属的活动性强弱判断正负极,要根据失电子难易程度确定负极,为易错点.

 中考解读考点精练系列答案
中考解读考点精练系列答案| A. | 长期饮用纯净水,有可能引起一些微量元素缺乏症 | |
| B. | 明矾既能沉降水中的悬浮物,又能杀菌消毒 | |
| C. | 合成洗涤剂和纯碱溶液都可洗去油污,二者去污原理相同 | |
| D. | 纤维素被食用进入人体内,在酶的作用下最终水解为葡萄糖为人体提供能量 |
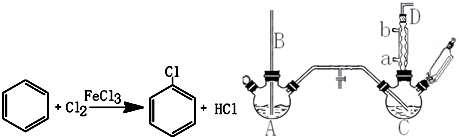
已知:氯苯为无色液体,沸点132.2℃.
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是平衡气压.冷凝管中冷水应从a(填“a”或“b”) 处通入.
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯.
①对C加热的方法是c(填序号)
酒精灯加热 b.油浴加热 c.水浴加热
②D出口的气体成分有HCl、苯蒸气和氯气.
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本.写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;HCl+NaOH=NaCl+H2O(写两个即可).
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是五氧化二磷或氯化钙.
(5)工业生产中苯的流失情况如下:
| 项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
| 苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
已知:N-N键能193kJ•mol-1,N≡N键能946kJ•mol-1
(1)按照轨道重叠方式可知,N2分子中共价键类型为σ键、π键,其中较稳定的是π键.
(2)合成氨常用铁系催化剂,写出基态铁原子价电子排布图
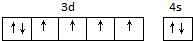 .
.(3)在较高温度下,铁对氮气的强化学吸附是合成氨速率的决定步骤.其中一种吸附方式为:
 ,该吸附方式能加快反应速率的原因是氮氮三键变成了双键,结构发生改变.
,该吸附方式能加快反应速率的原因是氮氮三键变成了双键,结构发生改变.(4)氨分子空间构型是三角锥,其氮原子采用的轨道杂化方式为sp3,氨是极性(填“极性”、“非极性”)分子,能与水分子形成氢键,易溶于水.固态氨是面心立方晶胞,有关数据如下表:
| X射线衍射 | N-H键长 | N-N距离 | H-N-H键角 |
| 数据 | 101.9pm | 339.0pm | 107° |
(6)列式计算固体氨的密度.
 如图是A分子的球棍模型和B分子的比例模型,回答下列问
如图是A分子的球棍模型和B分子的比例模型,回答下列问