题目内容
已知下列数据:
实验室制乙酸乙酯的主要步骤为:①在30mL的大试管中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合液;②连接装置,使产生的蒸气经导管通到试管所盛饱和Na2CO3溶液(加入1滴酚酞试液)上方2mm~3mm处,③小火加热试管中的混合液;④待小试管中收集约4mL产物时停止加热,撤出导管并用力振荡,然后静置待其分层;⑤分离出纯净的乙酸乙酯.请同学们回答下列问题:
(1)步骤①中,配制这一比例的混合液的操作是 .
(2)写出该反应的化学方程式 ,浓H2SO4的作用是 .
(3)步骤③中,用小火加热试管中的混合液,其原因 .
(4)步骤④所观察到的现象是
(5)步骤⑤中,分离出乙酸乙酯选用的仪器是 .
| 物 质 | 熔点/℃ | 沸点/℃ | 密度/g?cm-3 |
| 乙 醇 | -114 | 78 | 0.789 |
| 乙 酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.900 |
| 浓H2SO4 | 338 | 1.84 |
(1)步骤①中,配制这一比例的混合液的操作是
(2)写出该反应的化学方程式
(3)步骤③中,用小火加热试管中的混合液,其原因
(4)步骤④所观察到的现象是
(5)步骤⑤中,分离出乙酸乙酯选用的仪器是
考点:乙酸乙酯的制取
专题:实验设计题
分析:(1)添加试剂的顺序是先加入密度小的,再加入密度大的,浓硫酸的密度比乙醇大,所以后加,溶于水放热,须边加边摇放热混合;
(2)酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应;浓硫酸起到催化剂和吸水剂的作用;
(3)乙酸、乙醇的沸点低,易挥发;
(4)乙酸的酸性强于碳酸,饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层,乙酸乙酯在上层;
(5)根据乙酸乙酯的性质,选择实验方法和仪器进行解答;
(2)酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应;浓硫酸起到催化剂和吸水剂的作用;
(3)乙酸、乙醇的沸点低,易挥发;
(4)乙酸的酸性强于碳酸,饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层,乙酸乙酯在上层;
(5)根据乙酸乙酯的性质,选择实验方法和仪器进行解答;
解答:
解:(1)浓硫酸的密度比乙醇大,所以后加,溶于水放热,须边加边摇放热混合,所以配制乙酸、乙醇和浓硫酸的混合液的操作步骤是:先加乙醇4mL,再缓缓加入1mL浓H2SO4,边加边振荡,最后加4mL乙酸,
故答案为:先加乙醇4mL,再缓缓加入1mL浓H2SO4,边加边振荡,最后加4mL乙酸;
(2)酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应,所以乙酸脱羟基,乙醇脱氢离子,反应为:CH3COOH+C2H5OH CH3COOC2H5+H2O该反应为可逆反应,浓硫酸的作用为催化剂、吸水剂,吸水利于平衡向生成乙酸乙酯方向移动,
CH3COOC2H5+H2O该反应为可逆反应,浓硫酸的作用为催化剂、吸水剂,吸水利于平衡向生成乙酸乙酯方向移动,
故答案为:CH3COOH+C2H5OH CH3COOC2H5+H2O;催化剂、吸水剂;
CH3COOC2H5+H2O;催化剂、吸水剂;
(3)乙醇沸点78.0℃、乙酸的沸点117.9℃,它们的沸点较低,为防止乙醇、乙酸挥发,应小火加热,否则易造成原料的损失,
故答案为:乙酸、乙醇、乙酸乙酯沸点接近且较低,大火加热,反应物大量蒸发损;
(4)饱和碳酸钠溶液吸收挥发的乙醇,与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,乙酸乙酯密度比水小,在上层,因乙酸的酸性比碳酸强,所以乙酸能和碳酸钠反应生成二氧化碳气体,所以步骤④所观察到的现象是:在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄,
故答案为:在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄;
(5)乙酸乙酯浮在上层,分离油层和水层采用分液的方法即可,所以用到的仪器为分液漏斗,
故答案为:分液漏斗.
故答案为:先加乙醇4mL,再缓缓加入1mL浓H2SO4,边加边振荡,最后加4mL乙酸;
(2)酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应,所以乙酸脱羟基,乙醇脱氢离子,反应为:CH3COOH+C2H5OH
 CH3COOC2H5+H2O该反应为可逆反应,浓硫酸的作用为催化剂、吸水剂,吸水利于平衡向生成乙酸乙酯方向移动,
CH3COOC2H5+H2O该反应为可逆反应,浓硫酸的作用为催化剂、吸水剂,吸水利于平衡向生成乙酸乙酯方向移动,故答案为:CH3COOH+C2H5OH
 CH3COOC2H5+H2O;催化剂、吸水剂;
CH3COOC2H5+H2O;催化剂、吸水剂;(3)乙醇沸点78.0℃、乙酸的沸点117.9℃,它们的沸点较低,为防止乙醇、乙酸挥发,应小火加热,否则易造成原料的损失,
故答案为:乙酸、乙醇、乙酸乙酯沸点接近且较低,大火加热,反应物大量蒸发损;
(4)饱和碳酸钠溶液吸收挥发的乙醇,与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,乙酸乙酯密度比水小,在上层,因乙酸的酸性比碳酸强,所以乙酸能和碳酸钠反应生成二氧化碳气体,所以步骤④所观察到的现象是:在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄,
故答案为:在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄;
(5)乙酸乙酯浮在上层,分离油层和水层采用分液的方法即可,所以用到的仪器为分液漏斗,
故答案为:分液漏斗.
点评:本题考查了乙酸乙酯的性质及制备方法,注意把握乙酸乙酯的制备原理和实验方法,明确浓硫酸、饱和碳酸钠溶液在实验中的作用,题目难度不大.

练习册系列答案
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
有氧气参加的化学反应一定不属于( )
| A、复分解反应 |
| B、置换反应 |
| C、氧化还原反应 |
| D、离子反应 |
W、X、Y、Z是短周期元素,其部分性质如下表,下列说法正确的是( )
| W | 单质是淡黄色固体 | ||
| X | 在地壳中的含量居第二位 | ||
| Y | 原子最外层电子数是电子总数的
| ||
| Z | 第三周期原子半径最小的金属 |
| A、气态氢化物的热稳定性:X>W |
| B、最高价氧化物对应水化物的酸性:Y>X |
| C、离子半径:Z>W |
| D、Z的氧化物中含有非极性共价键 |
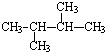
仅含一个三键的炔烃,氢化后的产物结构简式为 ,此炔烃可能有的结构有( )
,此炔烃可能有的结构有( )
 ,此炔烃可能有的结构有( )
,此炔烃可能有的结构有( )| A、1种 | B、2种 | C、3种 | D、4种 |
下列依据相关实验得出的结论正确的是( )
| A、加稀盐酸,产生的气体能使澄清石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| C、将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯 |
| D、滴加KSCN溶液,溶液不变色,再滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
能与Na反应放出H2,又能使溴水褪色,但不能使pH试纸变色的物质是( )
| A、CH2=CH-COOH |
| B、CH2=CH-CH2OH |
| C、CH2=CH-CH3 |
| D、CH2=CH-COOCH3 |



 +
+

