题目内容
6.在标准状况下,将CO2和CO的混合气体(标准状况下,该混合气体平均相对分子质量为32)充满一盛有足量Na2O2的容积为22.4L的密闭容器中,用间断的电火花引发至充分反应.反应完全后容器里的存在物叙述正确的是( )| A. | 存在0.5 mol的CO | B. | 存在0.25 mol的Na2CO3 | ||
| C. | 存在0.125 mol的O2 | D. | 存在0.75 mol的Na2CO3 |
分析 混合气体的平均摩尔质量为:M=32g/mol,设混合气体中CO为xmol,CO2为ymol,根据M=$\frac{28x+44y}{x+y}$=32计算二者的物质的量之比,进而计算体积比;由2CO+O2=2CO2,以及2CO2+2Na2O2=2Na2CO3+O2,二者相加可得CO+Na2O2=Na2CO3,反应后容器中存在的生成物为O2和Na2CO3,根据反应的化学方程式计算.
解答 解:混合气体的平均摩尔质量为:M=32g/mol,设混合气体中CO为xmol,CO2为ymol,由M=$\frac{28x+44y}{x+y}$=32可知x:y=3:1,
混合气体的物质的量为:$\frac{22.4L}{22.4L/mol}$=1mol,所以n(CO)=0.75mol、n(CO2)=0.25mol,
将2CO+O2=2CO2、2CO2+2Na2O2=2Na2CO3+O2相加可得CO+Na2O2=Na2CO3,由方程式关系可知:
CO+Na2O2=Na2CO3
0.75mol 0.75mol
2CO2+2Na2O2=2Na2CO3+O2
0.25mol 0.25mol 0.125mol
所以n(Na2CO3)=0.75mol+0.25mol=1mol,n(O2)=0.125mol,
故选C.
点评 本题考查混合物反应的计算,题目难度中等,侧重于学生的分析能力和计算能力的考查,本题注意利用CO+Na2O2=Na2CO3为解答该题的关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列过程中,共价键被破坏的是( )
| A. | 碘升华 | B. | 溴蒸气被木炭吸附 | ||
| C. | 蔗糖溶于水 | D. | 硫酸溶于水 |
1.下列描述的一定是金属元素的是( )
| A. | 易失去电子的物质 | B. | 原子核外有10个电子的微粒 | ||
| C. | 原子的最外层只有1个电子的元素 | D. | 原子核内有13个质子的元素 |
11.利用下列反应不能制得括号中纯净物质的是( )
| A. | 乙烯与氯气加成(1,2-二氯乙烷) | |
| B. | 乙烯与水加成(乙醇) | |
| C. | 等物质的量的氯气与乙烷在光照条件下反应(一氯乙烷) | |
| D. | 液溴与苯用溴化铁作催化剂反应(溴苯) |
16.下列说法正确的是( )
| A. | 反应:SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑,说明H2SiO3的酸性大于H2CO3的酸性 | |
| B. | 因为SO2具有漂白性,所以它能使品红溶液、溴水褪色 | |
| C. | 二氧化硅是生产光导纤维、玻璃的基本原料 | |
| D. | CO2、CH4、N2是温室气体 |
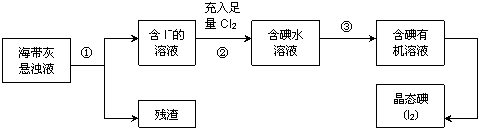
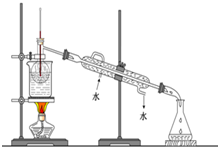
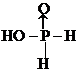 .H3PO2是一元(填“一”、“二”或“三”)酸.
.H3PO2是一元(填“一”、“二”或“三”)酸.