题目内容
下表为元素周期表的一部分,其中的字母代表对应的元素.
(1)M3+基态的电子排布式为 .
(2)元素Q位于元素周期表的 区.
(3)J、E、G的第一电离能由大到小的顺序为 ,电负性由大到小的顺序为 (用元素符号表示).
(4)LG4-的空间构型为
(5)已知几种共价键的键能数据如下表:
则1mol晶体J完全燃烧得到JG2所放出的热量为 .
| A | |||||||||||||||||
| D | E | G | |||||||||||||||
| J | L | ||||||||||||||||
| M | Q | ||||||||||||||||
(2)元素Q位于元素周期表的
(3)J、E、G的第一电离能由大到小的顺序为
(4)LG4-的空间构型为
(5)已知几种共价键的键能数据如下表:
| 化学键 | G-J | J-J | G=G |
| 键能/(KJ?mol-1) | 460 | 176 | 497 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置,可知A为氢、D为碳、E为氮、G为氧、J为Si、L为Cl、M为Fe、Q为Zn.
(1)根据能量最低原理书写Fe3+的核外电子排布式;
(2)元素Q位于元素周期表的ds区;
(3)非金属性越强,第一电离能越大,当元素原子各轨道处于半满、全满、全空时,能量较低,第一电离能高于同周期相邻元素;同周期自左而右电负性增大,同主族自上而下电负性减小;
(4)计算ClO4-离子中Cl原子价层电子对数,确定其空间构型;
(5)晶体Si属于原子晶体,每个Si原子形成4个Si-Si键,每个Si-Si键为Si原子提供
,则1mol晶体硅含有2molSi-Si键,二氧化硅也属于原子晶体,每个Si原子形成4个Si-O键,则1mol二氧化硅晶体硅含有4molSi-O键,结合键能计算.
(1)根据能量最低原理书写Fe3+的核外电子排布式;
(2)元素Q位于元素周期表的ds区;
(3)非金属性越强,第一电离能越大,当元素原子各轨道处于半满、全满、全空时,能量较低,第一电离能高于同周期相邻元素;同周期自左而右电负性增大,同主族自上而下电负性减小;
(4)计算ClO4-离子中Cl原子价层电子对数,确定其空间构型;
(5)晶体Si属于原子晶体,每个Si原子形成4个Si-Si键,每个Si-Si键为Si原子提供
| 1 |
| 2 |
解答:
解:由元素在周期表中位置,可知A为氢、D为碳、E为氮、G为氧、J为Si、L为Cl、M为Fe、Q为Zn.
(1)Fe3+基态的电子排布式为1s22s22p63s23p63d5,故答案为:1s22s22p63s23p63d5;
(2)由元素Q位于元素周期表位置可知,其位于周期表中ds区,故答案为:ds;
(3)非金属性越强,第一电离能越大,N元素原子2P轨道容纳3个电子,为半满稳定状态时,能量较低,第一电离能高于O元素,非金属性O>Si,故O元素第一电离能高于Si,故第一电离能N>O>Si;同周期自左而右电负性增大,同主族自上而下电负性减小,故电负性O>N>Si,
故答案为:N>O>Si;O>N>Si;
(4)ClO4-离子中Cl原子价层电子对数=4+
=4,其空间构型为正四面体,
故答案为:正四面体;
(5)发生反应Si+O2=SiO2,晶体Si属于原子晶体,每个Si原子形成4个Si-Si键,每个Si-Si键为Si原子提供
,则1mol晶体硅含有2molSi-Si键,二氧化硅也属于原子晶体,每个Si原子形成4个Si-O键,则1mol二氧化硅晶体硅含有4molSi-O键,故1mol晶体Si完全燃烧得到SiO2所放出的热量为:4mol×460kJ/mol-2mol×176kJ/mol-1mol×497kJ/mol=99lkJ,
故答案为:99lkJ.
(1)Fe3+基态的电子排布式为1s22s22p63s23p63d5,故答案为:1s22s22p63s23p63d5;
(2)由元素Q位于元素周期表位置可知,其位于周期表中ds区,故答案为:ds;
(3)非金属性越强,第一电离能越大,N元素原子2P轨道容纳3个电子,为半满稳定状态时,能量较低,第一电离能高于O元素,非金属性O>Si,故O元素第一电离能高于Si,故第一电离能N>O>Si;同周期自左而右电负性增大,同主族自上而下电负性减小,故电负性O>N>Si,
故答案为:N>O>Si;O>N>Si;
(4)ClO4-离子中Cl原子价层电子对数=4+
| 7-1-2×4 |
| 2 |
故答案为:正四面体;
(5)发生反应Si+O2=SiO2,晶体Si属于原子晶体,每个Si原子形成4个Si-Si键,每个Si-Si键为Si原子提供
| 1 |
| 2 |
故答案为:99lkJ.
点评:本题是对物质结构的考查,涉及元素周期表、核外电子排布、分子结构、反应热计算,难度中等,(5)为易错点、难点,根据晶体结构确定Si-Si键、Si-O键的物质的量是关键.

练习册系列答案
相关题目
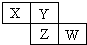 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )| A、氢化物的稳定性:X>Y |
| B、W的最高价氧化物对应水化物的酸性比Z的强 |
| C、Y的非金属性比X的强 |
| D、Y与Z形成的化合物是形成酸雨的主要物质 |
配置一定体积、一定物质的量浓度的NaOH溶液,下列情况对实验结果产生偏低影响的是( )
| A、容量瓶中原有少量水 |
| B、溶解所用的烧杯未洗涤 |
| C、定容时俯视 |
| D、溶解后立即注入容量瓶中 |
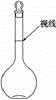 (3)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是
(3)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是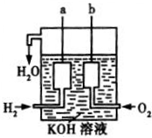 化学反应产生的各种能量是人类探索太空所需能量的重要来源.
化学反应产生的各种能量是人类探索太空所需能量的重要来源.